Le développement des stents actifs de dernière génération (DES) a permis de réduire nettement le risque de thrombose tardive, tout en maintenant un taux de resténose très bas. L’étude NORSTENT 1, publiée en 2016, confirme les excellents résultats des DES à 6 ans : taux de revascularisation de la lésion cible à 5.3% et taux de thrombose de stent à 0.8%.
Pour autant, la prévalence d’une néoathérosclérose tardive intrastent reste fréquente avec les DES de dernière génération (près de 50% sur les séries autopsiques). Cette prévalence est la même quelle que soit la génération du DES et semble dépendante de la durée d’implantation 2.
Il a été démontré que la néoathérosclérose est corrélée à la fois aux resténoses et aux thromboses tardives. Les mécanismes de formation de la néoathérosclérose intrastent ne sont pas totalement élucidés. Les hypothèses physiopathologiques évoquées sont la dysfonction endothéliale et les anomalies de flux liées à la présence du stent. La disparition totale de la structure métallique pourrait-elle éviter cette évolution ? Une résorption totale du stent après une période minimale « d’étayage » paraît ainsi séduisante.
Les autres avantages théoriques d’un stent résorbable (BVS : Bioresorbable Vascular Scaffold) seraient de respecter la vasoréactivité coronaire ou encore de permettre, en théorie, la réalisation d’un pontage aorto-coronarien au niveau de la zone traitée.
Considérations techniques
Composition d’un stent résorbable.
La structure du stent peut être polymérique (ABSORB® Abbott, DESOLVE® Elixir) ou métallique (MAGMARIS® Biotronik). Tous ces stents comportent un principe actif (limus). La durée idéale du temps de résorption n’est pas défi nie. Il ne doit pas être trop court pour maintenir l’étayage et la force radiale dans les premiers mois. Il ne doit pas être très long pour éviter les événements tardifs.
Le BVS ABSORB® est composé de deux couches de polymères résorbables : une couche d’acide polylactique L (PLLA) et une autre en PDLLA, plus superficielle, contenant le limus. La couche superfi cielle disparaît en quelques semaines, comme dans les DES de dernière génération. La couche profonde disparaît progressivement en 4 ans. La résistance des polymères est beaucoup plus faible que celle des stents métalliques. Pour compenser cela, les mailles du stent sont plus larges (191 microns pour ABSORB®) et plus épaisses (157 microns, contre environ 80 microns pour les DES actuels). Le challenge technologique sera d’affiner les mailles sans perdre en force radiale.
La composition du stent DESOLVE® est proche de celle de l’ABSORB®. La résorption se fait plus rapidement, en 2 ans, et l’épaisseur des mailles est de 150 microns.
Le stent MAGMARIS® est un stent composé d’un alliage résorbable composé à 95% de magnésium et d’une couche de PLLA contenant du sirolimus. La durée de résorption de la composante métallique est plus courte (60% à 6 mois, 96% à 1 an, 100% à 2 ans). De même que pour le BVS ABSORB®, et du fait d’une moindre résistance du matériau, un compromis a dû être réalisé en termes d’épaisseur (150 microns).
D’autres stents sont également en cours de développement.
Technique de pose
Les caractéristiques biomécaniques des BVS imposent une parfaite technique de pose. La stratégie « PSP » est recommandée : « Prepare the vessel, Size appropriately, Post dilate ».
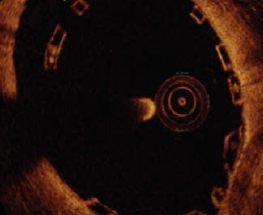
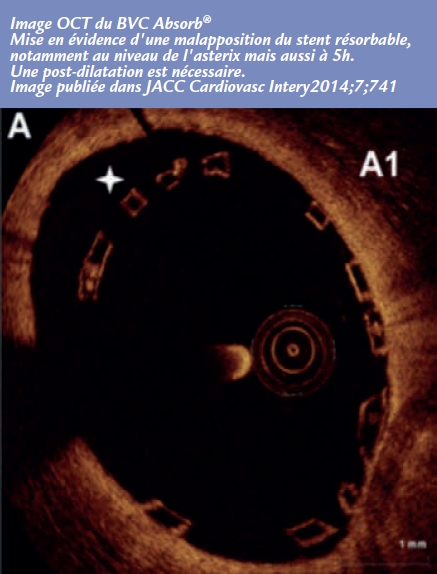
Le mauvais profil du stent lié à son épaisseur et sa plus faible force radiale rendent la prédilatation nécessaire. De même, la post-dilatation est systématique afin d’obtenir une parfaite apposition à la paroi du vaisseau de ce stent plus épais et moins compliant. Cependant, une post-dilatation excessive doit être évitée, car le BVS est plus propice à se fracturer. Ainsi, contrairement aux DES de dernière génération, dont le diamètre peut facilement être augmenté par post-dilatation, la faible déformabilité du BVS impose de choisir d’emblée la bonne taille. L’imagerie endocoronaire, telle l’OCT (Optical Coherence Tomography), est un outil très utile. Avant l’implantation du stent, elle permet de connaître exactement le diamètre de l’artère traitée et de choisir le bon diamètre de stent. Après la pose, elle détecte toute mal-apposition (Figure).
Quelle lésion traiter avec un BVS ?
L’épaisseur du BVS contre-indique son utilisation dans des artères de moins de 2.5 mm. Lors de la nécessité de poser 2 stents, il faudra proscrire toute superposition (overlapping), encore plus dans les petites artères. En effet, la réduction du diamètre de la lumière dans le cas d’un overlapping serait de 0.6 mm. Du fait de la moindre force radiale, il faut éviter de traiter les lésions calcifiées ou ostiales avec un BVS. En raison de son épaisseur, il est difficile de positionner un BVS dans une artère tortueuse ou rigide. Le BVS est à réserver aux lésions simples, non calcifiées, de calibre de 2.5 à 3.75 mm, sans bifurcation.
La lésion idéale semble être la rupture de plaque du sujet jeune, et la localisation idéale l’artère IVA, dans l’optique d’un éventuel pontage aorto-coronarien dans le futur.
Les études cliniques
Le stent le plus évalué est le BVS à l’évérolimus ABSORB® (Abbott Vascular). Dans les études « ABSORB », le BVS est comparé au DES Xience® (Abbott Vascular). Les résultats initiaux étaient encourageants pour le BVS mais un signal d’alerte a eu lieu en 2016, avec les résultats d’ABSORB II à 3 ans et d’ABSORB III à 2 ans. Les résultats de ces 2 études, avec un an de plus de recul, ont été présentés au congrès du TCT fin octobre 2017. Nous détaillerons ici surtout les données liées à la sécurité du stent.
L’étude ABSORB II 3
Dans cette étude randomisée en 2/1, 335 patients ont été traités par un ou plusieurs BVS ABSORB® et 166 patients par un ou plusieurs DES à l’évérolimus (Xience®, Abbott Vascular). Le critère principal de l’étude ABSORB II à 3 ans était l’étude de la vasoréactivité aux dérivés nitrés.
Étonnamment, aucune différence n’a été observée entre les 2 types de stents. Dans le groupe BVS, 3 thromboses de stents certaines ou probables sont survenues dans la première année, et 6 dans les deux années suivantes. Aucune thrombose n’a été rapportée avec le DES à 3 ans (3% vs 0%, p = 0,03). Il n’y avait cependant pas de différence de mortalité entre les 2 groupes, malgré une augmentation significative du risque d’infarctus dans le groupe BVS. Au récent congrès du TCT 2017, les résultats d’ABSORB II à 4 ans ont été présentés. Aucune thrombose n’est rapportée entre la troisième et la quatrième année dans le groupe BVS.
L’étude ABSORB III 4
Dans cette étude, 2008 patients ont également été randomisés en 2/1 BVS versus DES. Les résultats de l’étude ABSORB III à 3 ans ont été également récemment présentés au TCT. Le taux de thrombose de stent était de 2.8% dans le groupe BVS contre 0% dans le groupe DES (p=0.01). Il n’y avait pas de différence entre les 2 stents en termes de mortalité. A noter que, malgré des critères d’inclusion exigeant un diamètre minimal de référence de 2.5 mm, environ 20% des BVS ont été implantés dans des artères dont le diamètre était inférieur à 2.25 mm. La présence d’un BVS dans une petite artère était un facteur prédictif indépendant de thrombose de stent. Cependant, l’augmentation du risque de thrombose de stent était toujours présente dans la population de patients traités sur des artères d’un diamètre supérieur à 2.25 mm.
Les résultats à 30 jours de l’étude ABSORB IV ont été présentés au TCT 2017. Dans cette étude de 2590 patients, la technique d’angioplastie était plus rigoureuse avec 99,8% de pré-dilatation et 82,6% de post-dilatation. De plus, les patients porteurs de lésions sur de petits vaisseaux étaient exclus. À 30 jours, les résultats semblent un peu meilleurs que pour ABSORB III. Il existe cependant toujours une tendance à l’augmentation du risque de thrombose de stent (0,6% dans le groupe BVS vs 0.2%, p = 0.06). D’autres études testant le BVS ABSORB® ont également retrouvé un sur-risque de thrombose de stent comme l’étude AIDA 5.
Aucune étude randomisée n’a pour l’heure été réalisée avec les autres stents. Le stent MAGMARIS® (Biotronik) a été testé dans les registres BIOSOLVE. Dans BIOSOLVE II, le taux de thrombose de stent est de 0% à 2 ans sur les 123 patients 6. Le stent DESOLVE® (Elixir) a aussi été étudié dans un registre : les données étaient également rassurantes en terme de sécurité 7.
La qualité de l’implantation des BVS pourrait expliquer, en partie, ces résultats décevants. Plusieurs études vont dans ce sens. Très récemment et à partir des données des études ABSORB, il a été montré que la pré-dilatation, la post-dilatation et la bonne sélection du vaisseau (≤3.75 mm et ≥ 2.25 mm) sont trois facteurs indépendants corrélés à l’absence d’événements liés au BVS entre la première et la troisième année 8.
La durée de la double antiagrégation plaquettaire (DAPT) est aussi une question cruciale. Les événements tardifs observés dans les études cliniques incitent à poursuivre la DAPT au long cours et certaines études sont en faveur d’une diminution du risque de thrombose de stent sous DAPT comparativement à une mono antiagrégation 9. Le démantèlement du stent dans la phase de résorption pourrait être responsable d’une partie des événements tardifs. Ainsi, la DAPT pourrait être proposée jusqu’à la disparition complète du stent. Cette durée longue de DAPT (3 à 4 ans avec le BVS ABSORB) sera probablement un frein à l’utilisation des BVS, à moins que le temps de résorption diminue avec les nouvelles générations.
Conclusion
Actuellement, les BVS ne sont plus commercialisés et les patients implantés sont suivis dans le cadre de registres.
Les DES ont acquis une grande maturité, à la fois en terme d’efficacité et de sécurité, et mettre en évidence un bénéfice clinique face à ces dispositifs sera difficile.
Il existe cependant des raisons d’espérer quant au futur des BVS
• Le bénéfice potentiel des BVS par rapport aux DES sera peut être démontré sur le long terme, lorsque la néo-athérogénèse se développe au sein du stent métallique. Il est supputé que le sur-risque d’événements thrombotiques initiaux soit compensé au long cours par l’absence de néo-athérogénèse intrastent. Il convient donc d’attendre les données des études bien au-delà de 5 ans.
• La standardisation des techniques de pose et l’adaptation du traitement antiagrégant pourraient permettre d’améliorer la sécurité des BVS.
• D’autres générations de BVS sont en cours d’élaboration avec pour objectif d’améliorer leurs propriétés mécaniques.
Julien Jeanneteau,
Unité de Cardiologie Interventionnelle, Clinique St Joseph, Trélazé (Angers).
L’auteur déclare ne pas avoir de lien d’intérêt avec le sujet traité.
RÉFÉRENCES
1. Bonaa KH et al, N Engl J Med 2016;375:1242
3. Serruys PW et al, Lancet 2016;388:2479.
4. Kereiakes DJ et al, J Am Coll Cardiol. 2017 Oct 20.
5. Wykrzykowska JJ et al, N Engl J Med 2017 ;376(24):2319
6. Haude M et al, Lancet 2016 ;387(10013):31.
7. Abizaid A et al, JACC Cardiovasc Interv 2016 ;9(6):565.
8. Stone GW et al, J Am Coll Cardiol 2017 ;70(23):2863.
9. Felix CM et al. EuroInterv 2017 ;13(2):e177
