Les hypoglycémies ont toujours été un repoussoir majeur dans le traitement efficace du diabète : désagréables pour les patients même dans les formes mineures, contribuant à la dégradation de la qualité de vie, elles sont extrêmement impressionnantes pour les proches ou l’entourage professionnel quand elles sont sévères (c’est-à-dire plaçant le patient dans l’impossibilité de corriger lui-même l’hypoglycémie). Ces dernières formes sont aussi suspectes de mettre la vie des patients en danger, ce qui est avéré dans un nombre restreint de cas (dead-in-bed syndrome) et suspecté bien plus souvent. Elles ont longtemps été supposées inhérentes au traitement ambitieux du diabète et les recommandations récentes considèrent leur risque comme un argument pour rehausser l’objectif d’HbA1c chez certains patients, d’autant plus qu’ils sont fragiles.
Au milieu des années 2000, l’essai ACCORD a comparé chez des patients à haut risque cardiovasculaire une stratégie de contrôle glycémique intensif recourant notamment rapidement à une insulinothérapie multiinjections, à une stratégie conventionnelle. L’essai a été prématurément interrompu en 2008 par le comité indépendant de sécurité : une surmortalité dans le bras intensif était suggérée par l’analyse intermédiaire. La séquence “hypoglycémie sévère chez un patient fragile – souffrance myocardique – trouble du rythme – mort subite” a rapidement été proposée comme scénario du drame, une hypothèse soutenue par la plus grande fréquence des hypoglycémies notamment sévères dans le bras intensif. Dix ans plus tard, où en est-on du procès ?
Une controverse durable
La liste des arguments et contre-arguments s’est allongée avec le temps (Tableau 1). Cependant, ils sont indirects et en tirer une conclusion est affaire d’interprétation. S’il ne fait pas de doute que le principe d’un décès induit ou précipité par une hypoglycémie est possible (leur simultanéité a été observée chez un diabétique de type 1 qui portait un Holter glycémique pendant son sommeil, sans qu’aucune autre cause ne soit suspectée chez ce jeune homme), la question est quantitative : est-ce anecdotique ou fréquent dans une population fragile ? L’observation systématique d’une population diabétique à très haut risque cardiovasculaire et à risque d’hypoglycémies (donc avec insuline et/ou sulfamides), avec Holter glycémique 24/24 pendant des mois, pourrait permettre de capturer l’information glycémique au moment des événements cardiovasculaires, idéalement des décès cardiovasculaires. Le coût d’une telle étude serait très élevé, du fait du nombre de participants nécessaire.

Une alternative peut paraître encore plus utopique : réaliser un essai randomisant le même type de patients que ci-dessus, entre une stratégie médicamenteuse à haut risque d’hypoglycémies vs une stratégie à moindre risque, toutes choses étant égales par ailleurs en particulier l’équilibre glycémique ? Irréaliste, notamment parce qu’on ne peut espérer atteindre un même contrôle glycémique avec des stratégies aussi différentes ? C’est pourtant ce qui a été réalisé dans l’essai DEVOTE (Degludec vs Insulin Glargine in Patients with Type 2 Diabetes at High Risk of Cardiovascular Events), dont l’objectif primaire était autre il est vrai.
L’essai DEVOTE, reconstitution de la scène du crime
L’objectif primaire de cet essai était de démontrer la sécurité cardiovasculaire de l’insuline degludec, qui avait été mise en question par une analyse poolée de ses essais de développement de court terme. A la différence des autres médicaments antidiabétiques, les insulines ne sont pas réglementairement tenues de disposer d’un essai de sécurité cardiovasculaire.
Degludec est une nouvelle insuline lente, de très longue durée d’action, qui a été dessinée pour avoir une action encore plus stable que la glargine U100, l’insuline lente de référence à travers le monde depuis 15 ans. De fait, elle a démontré cet avantage pharmacodynamique, qui s’est traduit dans diverses populations par un bénéfice, tangible mais modeste, sur le risque d’hypoglycémies, la nuit essentiellement.
L’essai a comparé la degludec à l’insuline lente de référence, chez 7637 diabétiques à haut risque cardiovasculaire, (essentiellement en prévention secondaire). Il s’agissait d’un essai randomisé, en aveugle, en deux groupes parallèles partageant le même objectif très strict (trop, pour une telle population fragile ?) d’une glycémie entre 0,7 et 0,9 g/l le matin. La durée a été de deux ans environ.
L’HbA1c s’est améliorée en cours d’étude, de façon superposable dans les deux groupes. Ils n’ont pas différé non plus pour l’incidence du critère cardiovasculaire principal (composite d’infarctus du myocarde, AVC ou décès cardiovasculaire : 4,3/100 patients-années sous degludec (325 évènements) vs 4,8/100 sous le comparateur (356 événements), HR 0,91 [0,78-1,06]) ou chacun de ses composants, ni pour la mortalité.
Les facteurs de risque (poids, pression artérielle, lipides, fonction rénale) et les co-médications cardiovasculaires ont également été similaires dans les deux groupes. En revanche, du fait de ses propriétés pharmacodynamiques, il y a eu moins d’hypoglycémies sévères sous degludec : 3,7/100 patients-années sous degludec (280 évènements) vs 6,25/100 sous le comparateur (472 évènements), rapport des taux 0,60 [0,48-0,76].
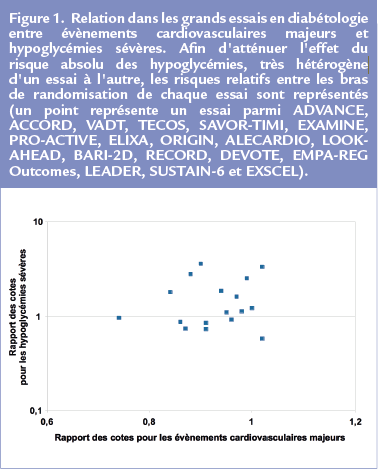
Bien que l’on ne puisse exclure que des épisodes d’hypoglycémies sévères aussitôt suivies d’un décès n’aient pas été identifiés et collectés correctement, modifiant à la marge les chiffres ci-dessus, cet essai a offert à la communauté une démonstration de la dissociation nette entre hypoglycémies sévères et événements cardiovasculaires majeurs. En fait, si l’on reprend les essais de grande taille dans le domaine du diabète, et que l’on met en relation les risques relatifs d’hypoglycémies sévères et les risques relatifs d’événementscardiovasculaires majeurs, on obtient un nuage de points non corrélés entre eux : cette dissociation semble générale (Figure 1).
Une histoire apaisée, et de nouveaux acteurs qui la rendent caduque
Que les hypoglycémies sévères ne soient pas pourvoyeuses en masse de morts cardiovasculaires est rassurant (les recommandations de la HAS placent les sulfamides en position prioritaire dans le choix thérapeutique), mais ne rend ni les diabétologues ni les patients plus tolérants à l’idée de les subir. Longtemps, cela a contribué à relâcher l’ambition du contrôle métabolique chez les patients à risque cardiovasculaire, ceux-là même pour qui la prévention est la plus pertinente.
Or, de nouvelles classes thérapeutiques ont rejoint la pharmacopée antidiabétique, en particulier les agonistes du récepteur du GLP-1 (injectables, une fois par jour ou une fois par semaine selon les formulations) et les inhibiteurs de SGLT2 (une prise orale quotidienne, actuellement non remboursées en France, mais disponible par exemple en Belgique). Ces deux classes aux modes d’action complètement différents, potentiellement associables, partagent des qualités : effet puissant sur la glycémie, réduction pondérale de quelques kilogrammes après quelques mois de traitement, réduction durable de quelques millimètres de mercure de la pression artérielle systolique, et surtout bénéfi ce cardiovasculaire suggéré par les essais réglementaires de sécurité. De plus, ils n’induisent ni l’un ni l’autre d’hypoglycémies par eux-mêmes. Il est souvent nécessaire, après une longue durée d’évolution du diabète, d’introduire de l’insuline pour compenser la défaillance progressive de l’insulinosécrétion. Cependant, ces nouvelles classes font que l’on peut facilement renoncer aux insulines rapides ou pré-mélangées, grosses pourvoyeuses d’hypoglycémies, en se contentant d’insuline lente à l’action bien plus prévisible et sûre, encore améliorée avec les insulines lentes de nouvelle génération.
Une combinaison metformine, insuline lente et agoniste du récepteur du GLP-1 est ainsi effi cace et sûre chez bon nombre de patients, en particulier en prévention cardiovasculaire secondaire. Ces progrès rendent pour l’essentiel caduque la controverse sur la relation entre hypoglycémies et risque cardiovasculaire.
Anisoara Bumbu 1 Ronan Roussel 1,2,3, Louis Potier 1,2,3
1 Département de diabétologie,endocrinologie, nutrition Hôpital Bichat Paris
2 INSERM, UMRS 1138, Centre de Recherche des Cordeliers, Paris
3 Université Paris Diderot, Sorbonne Paris Cité, UFR de Médecine, Paris
Les auteurs déclarent ne pas avoir de lien d’intérêt avec le sujet traité.
