TOTAL
Trial Of routine aspiration Thrombectomy with PCI versus PCI ALone in Patients with STEMI
Contexte et hypothèse
Les études TAPAS et TASTE, qui ont toutes deux évalué l’intérêt de la thrombectomie associée à l’angioplastie primaire en phase aiguë d’infarctus ont abouti à des résultats discordants. L’essai TOTAL a été mis en place pour apporter une réponse plus définitive à la question.
Critères d’inclusion et exclusion
Patients adressés pour angioplastie primaire dans les 12 heures suivant le début des symptômes d’un infarctus ST + (STEMI)
Plan d’étude et traitements étudiés
Étude randomisée ouverte, avec adjudication des événements en aveugle : angioplastie précédée d’une thrombectomie avec un système d’aspiration manuelle du thrombus (Export, Medtronic), ou angioplastie primaire directe (thrombectomie autorisée en tant que procédure de sauvetage).
Critères de jugement
Critère principal d’efficacité :
Décès cardiovasculaire, récidive d’infarctus, choc cardiogénique ou insuffisance cardiaque de classe IV NYHA à 180 jours.
Critères secondaires :
• Critère principal + thrombose de stent ou revascularisation du vaisseau cible à 180 jours
• Décès cardiovasculaire à 180 jours.
Critère principal de sécurité :
Accident vasculaire cérébral à 30 jours.
Analyses de sous-groupe préspécifiées :
Selon le volume du thrombus, la durée des symptômes, le flux TIMI initial, l’âge, la localisation de l’infarctus et le volume d’activité des centres participants.
Taille de l’échantillon et hypothèses statistiques
La taille de l’échantillon initialement prévue reposait sur un taux d’événements attendus de 14%. Après une analyse intermédiaire montrant un taux de 7% seulement, l’effectif a été porté à 10 700 patients, pour que l’étude ait une puissance de 80% de détecter un bénéfice de 20% sur le critère principal.
L’analyse principale repose sur une évaluation en intention- de-traiter modifiée en n’incluant que les patients effectivement traités par angioplastie primaire.
Des analyses secondaires (per-protocole, telles que traités et en intention de traiter non modifiée) étaient également prévues. La valeur de P pour considérer une différence comme significative est de 0,05.
Population
Recrutement de 10 732 patients dans 20 pays et 87 centres entre août 2010 et juillet 2014.
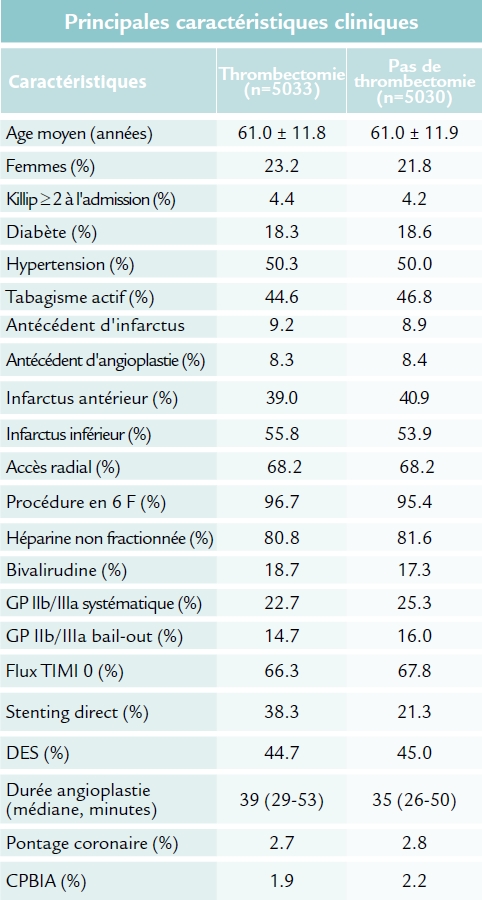
Résultats
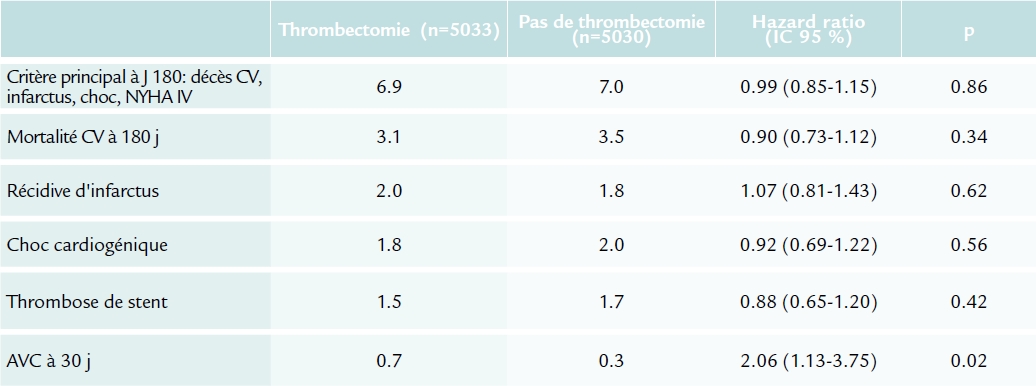
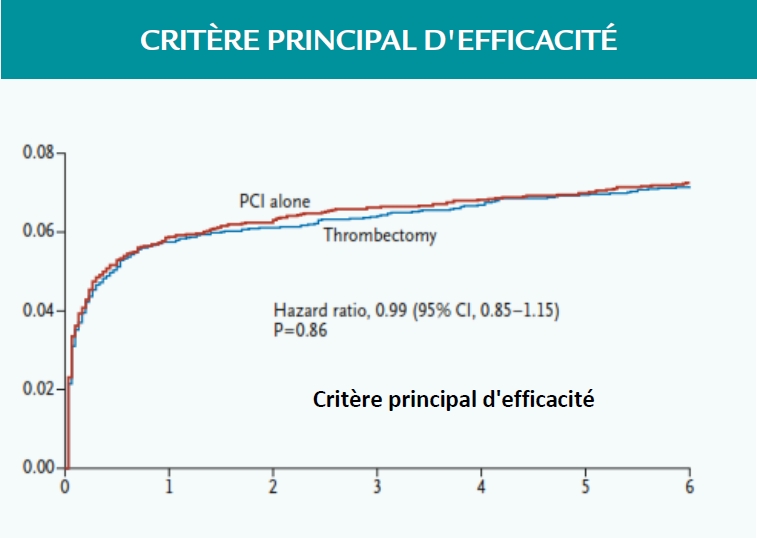
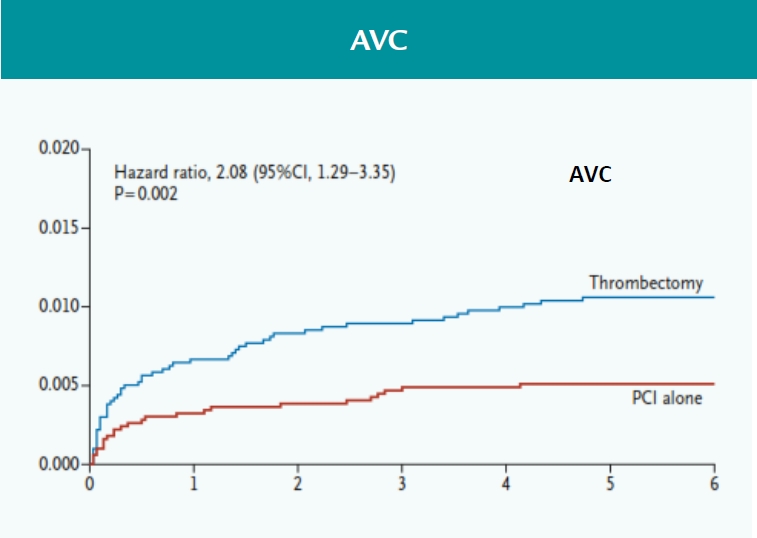
Analyses de sous-groupes :
Les résultats sont homogènes dans les différents sous-groupes étudiés.
Conclusion
L’utilisation systématique d’un dispositif de thrombectomie manuelle avant angioplastie primaire ne diminue pas le risque de mortalité cardiovasculaire, récidive d’infarctus ou insuffisance cardiaque sévère, mais majore le risque d’accident vasculaire cérébral.
Nicolas Danchin
RÉACTION
Les résultats ne prêtent pas à discussion
Chez les patients présentant un infarctus du myocarde en phase aiguë et qui bénéficient d’une angioplastie primaire, l’étude multicentrique TOTAL, randomisée ayant inclus 10 732 patients est la première étude d’aussi grande envergure.
Elle permet de confirmer que la thrombectomie manuelle systématique, comparée à l’angioplastie coronaire seule ne réduit pas à 6 mois le risque de mortalité cardio-vasculaire, la récidive d’infarctus du myocarde, le choc cardiogénique ou l’insuffisance cardiaque classe IV selon la classification NYHA mais par contre augmente le risque d’Accident Vasculaire Cérébral.
Pourquoi de tels résultats ?
Les études TAPAS, TASTE et INFUSE-AMI étaient concordantes pour retrouver dans le groupe thrombectomie une amélioration significative en termes de résolution du segment ST et d’embolisation distale.
Seule l’étude TAPAS monocentrique s’accompagnait d’une réduction de la mortalité. L’étude TOTAL retrouve la même amélioration au niveau du segment ST et de l’embolisation distale mais une fois de plus ces résultats à très large échelle ne se traduisent pas en termes de réduction de la mortalité cardiaque et/ou d’évènements cardio-vasculaires majeurs. Force est de constater que l’amélioration de l’ECG voire la perfusion coronaire distale sont des paramètres insuffisants pour réduire les évènements cardiaques majeurs.
De plus le risque d’AVC augmente de façon significative (HR 2.06, p<0.015) à 1 et 6 mois comme le soulignait déjà la méta-analyse d’études randomisées en 2010. Même si le nombre de passages de thrombo-aspiration n’est pas mentionné et que le ou les mécanismes d’AVC ne sont pas encore élucidés, l’hypothèse d’embolisations thrombotique ou gazeuse, au moins dans les 24 premières heures, semble prendre toute sa valeur.
La technique de thrombo-aspiration en l’état actuel doit-elle être définitivement abandonnée ?
Il est sûr que ces résultats globaux n’incitent plus à thrombo-aspirer systématiquement les artères coupables en phase aigüe d’infarctus. Les sceptiques diront que l’étude n’était pas réalisée en aveugle pour les cardiologues interventionnels, preuve de plus d’antiGP2B3A dans le groupe angioplastie seule, que c’était une étude de thrombectomie systématique et non pas sélective, que dans le bras contrôle il y a eu 7% de thrombectomie en bail-out pour échec d’angioplastie seule, que l’étude n’était pas conçue pour tester l’efficacité du bail-out et que le cathéter 6F (> 95% des cas) est discutable de par le diamètre trop faible de sa lumière interne.
Tous ces arguments peuvent être entendus mais il semble raisonnable de penser qu’en dehors d’une situation de bail-out ou d’un flux TIMI 0 ou 1 avec volumineux thrombus au moment de débuter l’angioplastie primaire, la thrombectomie systématique lors de la phase aiguë d’infarctus n’a plus sa raison d’être.
Peut-on dire plus jamais ?
Le concept depuis une dizaine d’années semblait séduisant et si nous étions encore dans les années 2000 sans véritable étude randomisée, multicentrique à large échelle, tous les cardiologues interventionnels continueraient à vanter les mérites de cette technique. La preuve est apportée par la prolifération des cathéters de thrombo-aspiration actuellement disponibles sur le marché. La médecine nous a bien appris depuis longtemps que ce n’était pas une science exacte et qu’il fallait toujours raison garder. Peut-être que le mécanisme d’aspirer simplement le thrombus est insuffisant, même s’il paraissait séduisant. Peut-être faut-il mieux cibler les sous-groupes redevables de cette technique ou peut-être faut-il totalement modifier le concept actuel ? L’avenir nous dira donc très prochainement ce que feront les cardiologues interventionnels et les industriels vis-à-vis de cette technique… et d’une prochaine révolution interventionnelle à venir.
Didier CARRIÉ,
CHU Rangueil, Toulouse
Article paru dans le CORDIAM N°5 (Avril 2015)
Télécharger l’article
