La fibrillation atriale est la forme d’arythmie la plus fréquente avec une prévalence de l’ordre de 1 à 2% de la population et dont l’incidence augmente fortement avec l’âge. Son impact majeur en termes de complications est essentiellement lié à la survenue de complications thrombo-emboliques dont l’évaluation du risque repose sur le calcul du score clinique CHADS-VASC. Lorsque ce score est supérieur à 1, il existe théoriquement une indication à un traitement anticoagulant oral.
Or un nombre important de patients, notamment parmi les plus âgés présentent des contre-indications formelles à une anticoagulation curative.
Introduction
La survenue de thrombi atriaux est liée à la stase sanguine dans l’oreillette du fait de la perte de contraction chez les patients en fibrillation atriale, qui favorise alors l’activation de la cascade de la coagulation. L’auricule, appendice atrial situé à la face antéro-latérale de l’oreillette gauche, est une zone préférentielle de constitution des thrombi.
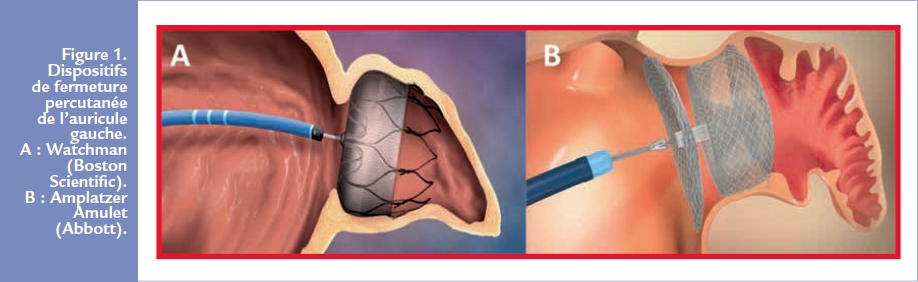
Afin de protéger du risque embolique les patients présentant une contre-indication au traitement anticoagulant, des dispositifs d’occlusion de l’auricule gauche ont été développés. Actuellement, deux dispositifs sont commercialisés : le Watchman® (Boston Scientific) et l’Amplatzer® Amulet® (Abbott) Figure 1.
La procédure d’occlusion percutanée de l’auricule gauche fait désormais partie de l’arsenal thérapeutique de la fi brillation avec une place bien défi nie dans les recommandations de la Société Européenne de Cardiologie avec un niveau de recommandation IIb et de preuve B 1, ainsi qu’un rapport de la Haute Autorité de Santé et un consensus d’expert de la Société Française de Cardiologie 2.
Les données de la littérature
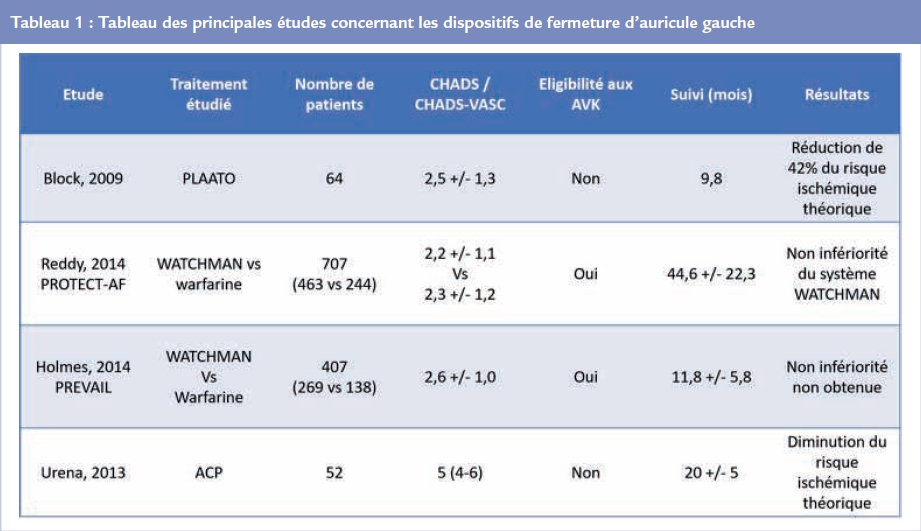
Les premières preuves de concept ont été apportées en 2005 avec le système PLAATO® (EV3). Une première étude de faisabilité, puis des résultats à long terme 3 ont permis de montrer une incidence diminuée de complications thrombo-emboliques chez des patients contre-indiqués pour une anticoagulation curative. Ce système n’est cependant plus commercialisé de nos jours. Le dispositif Watchman® a été le premier à être comparé à l’anticoagulation curative dans une étude randomisée. Il s’agit de l’étude PROTECT-AF, qui comparait chez 707 patients porteurs d’une FA non valvulaire, l’implantation du système Watchman® versus un traitement anticoagulant par warfarine. A 18 mois de suivi, il n’y avait pas de différence significative entre les deux approches thérapeutiques concernant la survenue d’embolies systémiques 4.
Concernant le dispositif Amulet®, une étude randomisée versus traitement anticoagulant curatif sur 1000 patients, présentée en 2017, retrouvait des résultats similaires entre les deux groupes sur la prévention des embolies systémiques. Nous disposons également de plusieurs
séries de patients ayant une contre-indication formelle à une anticoagulation curative chez qui une diminution de l’incidence d’événements thrombo-emboliques après occlusion de l’auricule gauche était retrouvée 5.
Enfin, une méta analyse reprenant l’ensemble des études randomisées avec tous les dispositifs de fermeture d’auricule gauche a récemment démontré une efficacité tendant à être similaire à celle de l’anticoagulation orale ainsi qu’une supériorité par rapport à la double anti-agrégation plaquettaire pour la prévention des événements thromboemboliques 6. Cette méta analyse a par ailleurs logiquement retrouvé une diminution du risque hémorragique après fermeture de l’auricule.
Quels sont les patients concernés ?
Du fait du faible nombre d’essais randomisés Tableau 1, les recommandations européennes et françaises limitent l’implantation de ces dispositifs aux patients à haut risque embolique (score de CHADS-VASC supérieur ou égal à 4), présentant par ailleurs une contre-indication formelle à l’anticoagulation curative (score de HAS-BLED supérieur ou égal à 3) Tableau 2.

L’indication doit être posée en concertation multidisciplinaire incluant l’avis d’un cardiologue interventionnel, d’un anesthésiste-réanimateur et d’un spécialiste de l’organe responsable de la contre-indication aux anticoagulants. Il faut également noter que le refus par le patient d’un traitement anticoagulant ne constitue pas, selon les recommandations, une indication à la fermeture de l’auricule.
Quel est le bénéfice attendu et pour quels risques ?
Le principal bénéfice attendu de la fermeture d’auricule est la diminution du risque ischémique embolique notamment chez les patients ne pouvant bénéficier des traitements anticoagulant oraux. Cette diminution ressort clairement dans la littérature, ainsi qu’un réel bénéfice par rapport à l’antiagrégation plaquettaire qui, comme on le sait, n’a désormais plus d’indication chez le patient en fibrillation atriale. L’occlusion de l’auricule gauche permet également de réduire significativement le risque hémorragique des patients malgré la nécessité de poursuivre, le plus souvent transitoirement, les traitements anti-agrégants après implantation.
S’agissant d’une procédure invasive, il existe des complications qui restent rares. Dans une méta analyse reprenant les principales études sur les fermetures d’auricule 6, un taux de succès d’implantation autour de 98% était retrouvé. Les principales complications observées sont comparables entre les différents systèmes d’occlusion.
La complication la plus fréquente est la survenue d’un épanchement péricardique (2 à 3%) nécessitant parfois un drainage en urgence. Il existe également un risque d’accident ischémique pendant la procédure, malgré l’anticoagulation préventive, ainsi qu’un risque de complications au niveau du point de ponction. Il faut cependant noter que l’incidence de ces complications diminue avec la courbe d’apprentissage, le perfectionnement des techniques d’implantation et du matériel. A long terme, les complications les plus fréquentes sont les fuites para-prothétiques résiduelles (1,9%) et la thrombose du dispositif (4,4% dans l’étude PROTECTAF), sans relation toutefois avec la survenue d’événements indésirables associés.
Aspects pratiques
Réalisation d’une fermeture percutanée de fermeture d’auricule
Après l’indication retenue en concertation multidisciplinaire, un bilan préopératoire est alors nécessaire. Outre les examens classiques devant précéder une anesthésie générale, il est nécessaire de vérifier l’absence de thrombus intra-auriculaire avant la procédure ainsi que d’évaluer la morphologie et la taille de l’auricule gauche et sa compatibilité avec les dispositifs de fermeture.
Le scanner de l’auricule gauche est aujourd’hui considéré comme l’examen de référence pour visualiser l’auricule gauche Figure 2. Il nécessite cependant une injection de produit de contraste et peut, en cas de contre-indication, être éventuellement remplacé par une échographie transoesophagienne (ETO) préopératoire. En cas d’évaluation par ETO, la reconstruction de l’auricule en 3 dimensions est utile pour la compréhension de son anatomie complexe.
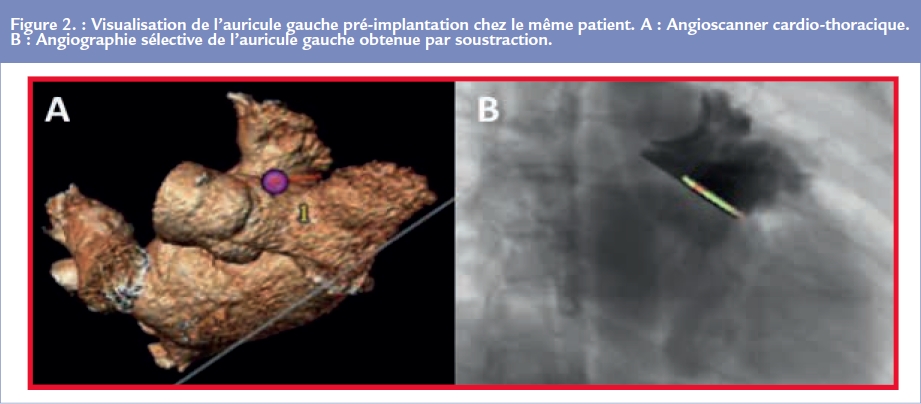
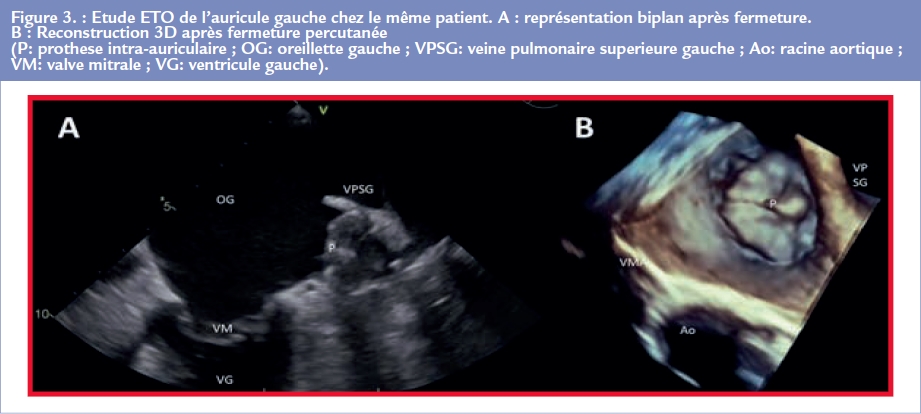
La procédure de fermeture est réalisée, sous anesthésie générale et anticoagulation préventive, dans un centre de cardiologie interventionnelle, avec une couverture chirurgicale sur site. Le geste est guidé par fluoroscopie et ETO simultanée. Après ponction veineuse fémorale, l’oreillette gauche est abordée par voie transseptale. Une angiographie de l’auricule gauche est alors réalisée pour évaluer son anatomie et le diamètre maximal de son collet sous différentes projections Figure 2. Ces mesures sont confirmées par l’ETO et permettent ainsi le choix d’une taille de prothèse adaptée. Celle-ci est ensuite déployée à l’entrée de l’auricule gauche, au niveau du collet, toujours sous contrôle ETO Figure 3 et fluoroscopique pour s’assurer de son bon déploiement et vérifier l’absence de conflit avec les autres structures intracardiaques, ou de fuite résiduelle intra ou paraprothétique. Un test de stabilité par légère traction est également réalisé avant de libérer définitivement la prothèse.
Prise en charge après implantation
Une surveillance régulière par ETO ou scanographique de l’auricule gauche est nécessaire pour évaluer la présence de fuites résiduelles et surtout la formation secondaire de thrombus. Un premier contrôle est généralement réalisé dans les 2 à 3 mois suivant l’implantation puis à un et deux ans en l’absence d’événement intercurrent.
Sur le plan thérapeutique, un traitement anti-agrégant plaquettaire doit être initié le jour précédant l’implantation puis poursuivi pour une durée théorique d’au moins 6 mois. Ce schéma peut toutefois être adapté en fonction du risque hémorragique des patients.
Il faut également savoir qu’une antibioprophylaxie de l’endocardite infectieuse doit être effectuée avant tout geste à risque dans les 6 mois suivant la procédure d’implantation.
Synthèse
• La fermeture de l’auricule gauche est une procédure permettant de prévenir la survenue de complications thrombo-emboliques dans la fibrillation atriale non valvulaire.
• Elle est pour l’instant réservée aux patients à haut risque embolique (score de CHADS-VASC supérieur ou égal à 4) et présentant une contre-indication formelle à une anticoagulation au long cours.
• L’indication d’implantation doit être retenue au cours d’une concertation multidisciplinaire.
• Le bilan préopératoire comprend systématiquement une évaluation ETO ou scanographique de la morphologie et de la taille de l’auricule gauche afin d’adapter au mieux le modèle de prothèse.
• La plus fréquente complication de cette procédure est la survenue d’un épanchement péricardique potentiellement compressif pouvant nécessiter un drainage en urgence.
Quentin Voglimacci, Nicolas Combes, Stéphane Combes, Anne-Sophie Béraud, Fleur Descoutures, Christèle Cardin, Zeynab Jebberi, Thomas Vacter, Arthur Azemar, Gérôme Pineaud, Jean-Paul Albenque, Serge Boveda. Département de Rythmologie, Clinique Pasteur, Toulouse.
L’auteur déclare ne pas avoir de lien d’intérêt avec le sujet traité. S. Boveda est consultant chez Boston Scientific.
RÉFÉRENCES
1. Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, et al. 2016 ESC Guidelines for the management of atrial fi brillation developed in collaboration with EACTS. Eur Heart J. 2016 Oct 7;37(38):2893–962.
2. Percutaneous occlusion of the left atrial appendage: An expert consensus statement. Arch Cardiovasc Dis. 2015 Aug;108(8–9):460–7.
3. Block PC, Burstein S, Casale PN, Kramer PH, Teirstein P, Williams DO, et al. Percutaneous Left Atrial Appendage Occlusion for Patients in Atrial Fibrillation Suboptimal for Warfarin Therapy. JACC Cardiovasc Interv. 2009 Jul;2(7):594–600.
4. Reddy VY, Doshi SK, Sievert H, Buchbinder M, Neuzil P, Huber K, et al. Percutaneous Left Atrial Appendage Closure for Stroke Prophylaxis in Patients With Atrial Fibrillation: 2.3-Year Follow-up of the PROTECT AF (Watchman Left Atrial Appendage System for Embolic Protection in Patients With Atrial Fibrillation) Trial. Circulation. 2013 Feb 12;127(6):720–9.
5. Urena M, Rodés-Cabau J, Freixa X, Saw J, Webb JG, Freeman M, et al. Percutaneous Left Atrial Appendage Closure With the AMPLATZER Cardiac Plug Device in Patients With Nonvalvular Atrial Fibrillation and Contraindications to Anticoagulation Therapy. J Am Coll Cardiol. 2013 Jul;62(2):96–102.
6. Sahay S, Nombela-Franco L, Rodes-Cabau J, Jimenez-Quevedo P, Salinas P, Biagioni C, et al. Effi cacy and safety of left atrial appendage closure versus medical treatment in atrial fi brillation: a network metaanalysis from randomised trials. Heart. 2017 Jan 15;103(2):139–47.
