Les nouvelles recommandations de 2017 reprennent point par point le diagnostic et la prise en charge de lésions à chaque étage artériel, à l’exclusion de l’aorte et des artères coronaires, en se focalisant sur les causes athéromateuses, 6 ans après les premières recommandations de l’ESC sur le sujet 1.
Ce document regroupe des présentations cliniques variées, ayant de nombreuses similitudes de par la nécessité de la réduction du risque ischémique.
Une équipe vasculaire, composée de médecins vasculaires, de cardiologues, de chirurgiens vasculaires et de radiologues est fondamentale et nécessaire afin de coordonner la prise en charge de ces patients. Le traitement médical optimal pour ces différentes localisations reste commun.
Il regroupe la diminution des facteurs de risque cardiovasculaire (dont principalement le sevrage tabagique, le contrôle de la pression artérielle, l’équilibration du diabète), et le plus souvent la prescription d’une antiagrégation plaquettaire simple au long cours, de statines et d’IEC ou d’ARA2.
Artériopathie des membres inférieurs
Arthériopathie chronique
Le dépistage de l’artériopathie chronique des membres inférieurs (AMI) repose sur la mesure de l’index de pression systolique (IPS), rapport de pression systolique entre la cheville et le bras, mesurée par Doppler continu. L’écho-Doppler artériel est ensuite le premier examen complémentaire utile pour confirmer le diagnostic (sans oublier l’évaluation de l’aorte abdominale pour le dépistage de l’anévrysme de l’aorte abdominale). Lorsqu’ une revascularisation est nécessaire, le bilan doit être complété par une imagerie globale, par tomodensitométrie (TDM) ou angiographie par résonance magnétique (ARM).
La prise en charge dépend de la symptomatologie du patient, répartie en trois groupes : atteinte asymptomatique, claudication intermittente, ischémie critique. En cas de découverte fortuite d’un IPS inférieur à 0,9 ou de l’abolition d’un pouls, une évaluation standardisée du périmètre de marche est recommandée avant de conclure à une atteinte asymptomatique. En effet, de nombreux patients présentent une AMI « masquée » révélée par le test de marche sur tapis roulant. Dans ce cas, la prise en charge requise est similaire à celle de la claudication.
Outre l’arrêt impératif du tabagisme actif ou passif, le traitement médical ne s’adresse qu’aux patients présentant une AMI symptomatique ou masquée. Il comporte une simple antiagrégation plaquettaire, l’utilisation de statines, avec un bénéfice prouvé sur l’amélioration du périmètre de marche, et d’IEC ou ARA2.
Prise en charge de la claudication intermittente
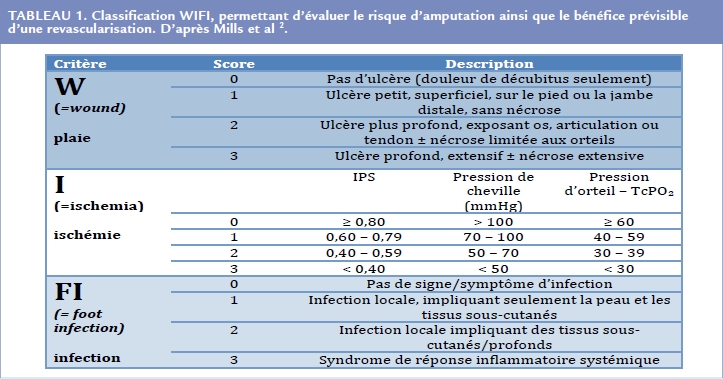
En cas de claudication intermittente, le traitement médical avec une rééducation vasculaire supervisé est recommandé, quels que soient l’extension et le retentissement hémodynamique des sténoses artérielles. La revascularisation n’intervient qu’en deuxième ligne de traitement, soit du fait d’une amélioration insuffisante après rééducation vasculaire, soit d’emblée, en cas d’altérations sévères de la qualité de vie (classe IIa).
Le choix de la revascularisation (endovasculaire ou chirurgie ouverte) dépend de l’étage et de la longueur de la portion atteinte, selon le schéma Figure 1. Dans tous les cas, une décision multidisciplinaire par une équipe vasculaire est requise. La règle étant de réserver cette revascularisation aux lésions aortoiliaques et fémorales.
Prise en charge de l’ischémie critique ou ischémie chronique menaçant le membre inférieur
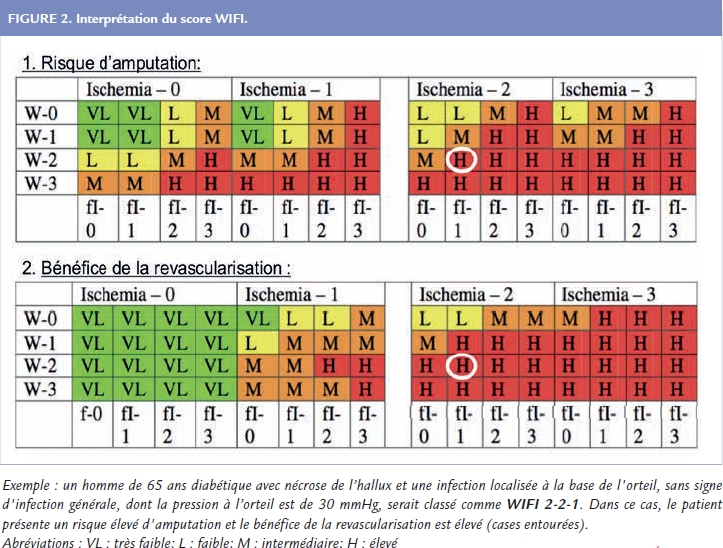
Ce stade clinique est désormais dénommé « Chronic limb-threatening ischaemia », correspondant à une ischémie chronique menaçant le membre inférieur, afin de mieux souligner le risque local de ce stade d’évolution de la maladie. Les recommandations encouragent l’utilisation généralisée de la classification WIFI (Wound, Ischaemia, Foot Infection) évaluant la gravité de l’ischémie critique.
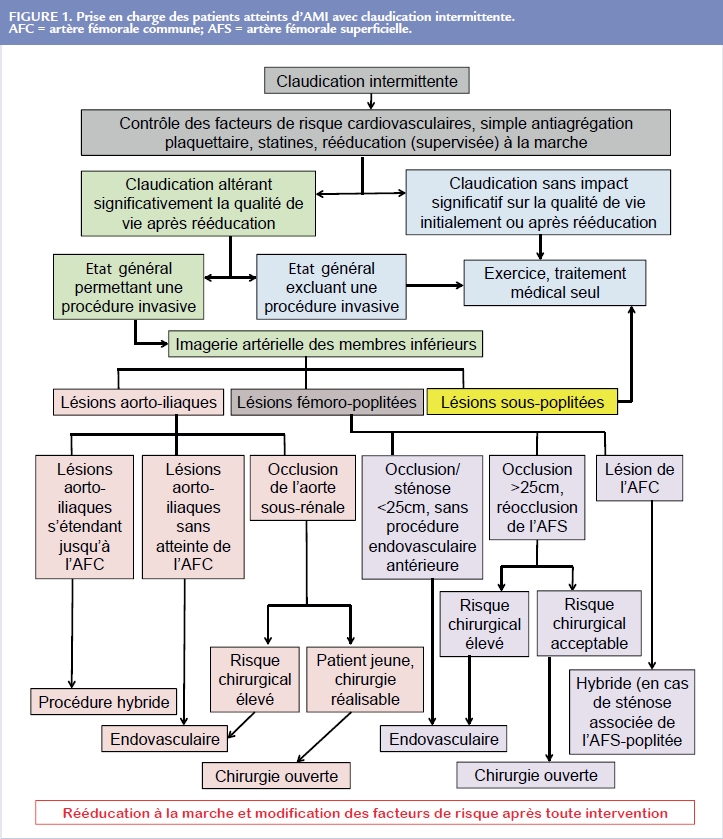
Elle permet de mieux évaluer le risque d’amputation ainsi que le bénéfice attendu d’une revascularisation.
Après réalisation du score, l’interprétation se fait à l’aide des deux tableaux fournis en Figure 2 ou par une application en ligne. Quel que soit le stade de l’ischémie critique, une revascularisation doit être tentée le plus souvent possible en plus du traitement médical.
L’amputation, en combinaison avec une procédure de revascularisation, reste souvent nécessaire en première intention dans les cas de nécrose extensive ou de gangrène. Dans ces cas, une amputation sous-gonale est préférable pour conserver l’articulation du genou.
Gestion du traitement antiagrégant plaquettaire et anticoagulant
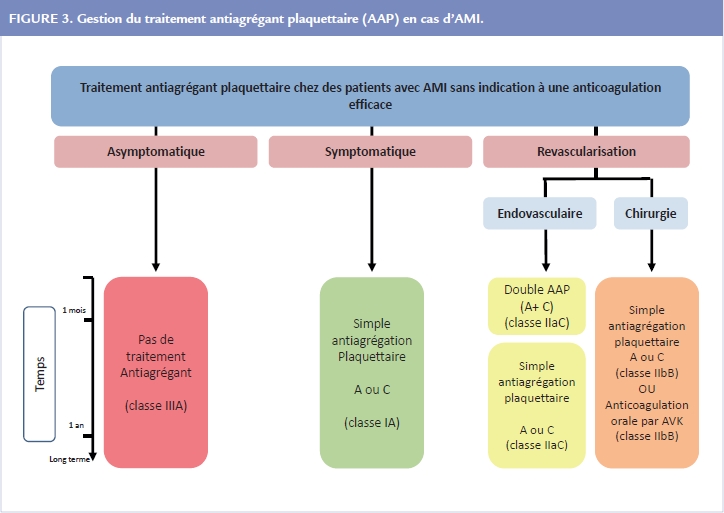
Une simple anti-agrégation plaquettaire est recommandée au long cours (classe I), par aspirine ou clopidogrel avec une préférence pour le clopidogrel (classe IIb) chez tout patient avec AMI symptomatique.
Aucun traitement n’est en revanche recommandé chez le patient asymptomatique (classe III). La double antiagrégation par aspirine + clopidogrel n’est recommandée qu’en cas de stenting infra-inguinal, au moins pendant 1 mois.
Les interventions de revascularisation sans pose de stent ne nécessitent qu’une simple antiagrégation plaquettaire au long cours. En cas de pontage, le traitement par AVK (INR cible entre 2 et 3) ne semble pas supérieur à l’utilisation d’aspirine seule Figure 3.
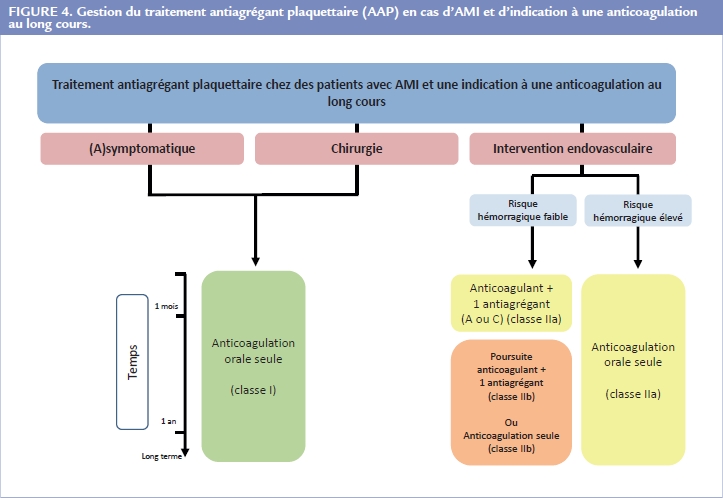
Des recommandations spécifiques concernant les patients sous anticoagulation au long cours facilitent le choix dans les situations combinant anticoagulation et antiagrégation plaquettaire Figure 4. Les anticoagulants oraux directs (AOD) peuvent être maintenus en cas d’AMI. Après revascularisation, l’anticoagulation orale peut être couplée à 1 mois de simple antiagrégation plaquettaire en cas de faible risque hémorragique. En cas de risque élevé, seuls les anticoagulants seront maintenus.
Enfin, les résultats de l’étude COMPASS concernant l’utilisation associée du rivaroxaban en plus de l’aspirine n’ont pas été inclus dans ces recommandations, car publiés seulement en septembre 2017. Ils semblent donner l’avantage au traitement par rivaroxaban 2,5mg x2/jour et aspirine 3.
Ischémie aiguë
Après le diagnostic clinique, une anticoagulation par héparine sodique associée à un traitement antalgique efficace doit être immédiatement débutée. La revascularisation est toujours une urgence thérapeutique. Une imagerie diagnostique avant la revascularisation ne sera réalisée qu’en l’absence de déficit sensitivomoteur. Dans le cas contraire, aucun examen complémentaire ne doit retarder la revascularisation.
Atteinte des troncs supra-aortiques
Pathologie carotidienne
Le diagnostic de sténose carotidienne sera préférentiellement réalisé par écho-Doppler. Une angiographie par résonnance magnétique (ARM) ou un angioscanner sont également possibles afin d’évaluer le degré de sévérité et l’extension de la sténose. Le bilan avant revascularisation carotidienne nécessite systématiquement une imagerie complémentaire à l’écho-Doppler (par ARM ou scanner).
En cas de sténose asymptomatique, du fait d’un bénéfice faiblement démontré, une revascularisation, à partir d’un degré de sténose ≥60% (en méthode NASCET) ne doit pas être systématiquement proposée. La décision d’une revascularisation doit prendre en compte une évaluation individualisée en termes de risque d’AVC, de risque de l’intervention et de l’espérance de vie du patient.
En cas de sténose symptomatique (avec confirmation d’un AVC ou AIT ipsilatéral récent), une revascularisation carotidienne est indiquée systématiquement en cas de sténose ≥70% (en méthode NASCET). Elle peut également être proposée en cas de sténose intermédiaire, entre 50 et 70%, seulement après prise en compte du risque individuel du patient. Lorsque une revascularisation est indiquée, celle-ci doit être réalisée rapidement, dans les 14 jours. En revanche, il n’y a pas d’indication à une revascularisation pour des plaques de moins de 50%.
L’endartériectomie carotidienne reste la procédure de choix pour la revascularisation carotidienne, que la sténose soit symptomatique ou non. L’angioplastie avec pose d’un stent reste l’alternative en cas de risque chirurgical élevé (notamment pour les patients de plus de 80 ans, présentant des comorbidités cardiaques ou pulmonaires).
Une simple antiagrégation plaquettaire est nécessaire en cas de sténose carotidienne (symptomatique ou non). La double antiagrégation plaquettaire ne sera recommandée qu’après angioplastie-stenting, pendant 1 mois.
Pathologie vertébrale
La pathologie artérielle vertébrale est moins codifiée. En dehors du traitement médical habituel, une revascularisation chirurgicale ne sera proposée qu’en cas de sténose symptomatique avec récidives ischémiques sous traitement médical.
Atteinte artérielle des membres supérieurs
L’atteinte athéromateuse des membres supérieurs est préférentiellement proximale. Le diagnostic est réalisé soit par écho-Doppler, par ARM ou TDM. Seul un traitement médical est habituellement nécessaire.
Une revascularisation ne peut être proposée que pour les patients présentant des symptômes sévères, en cas de présence d’une fi stule artério-veineuse de dialyse, ou bien en cas de pontage aorto-coronaire prévu, afin d’améliorer le flux de l’artère mammaire interne. Une procédure endovasculaire ou une chirurgie ouverte devront être discutées en équipe vasculaire.
Atteinte mésentérique
Ischémie mésentérique aiguë
Il s’agit d’une urgence thérapeutique avec une forte mortalité, d’environ 80%, en l’absence de revascularisation précoce. Pour cette raison, l’imagerie de choix est tout d’abord l’angioscanner abdominal, en temps artériel et veineux. Une fois le diagnostic confirmé, une revascularisation doit être réalisée le plus rapidement possible. La voie endovasculaire sera préférentiellement utilisée en cas d’occlusion thrombotique. Procédure endovasculaire et chirurgie ouverte semblent équivalentes en cas d’occlusion embolique. Même en cas de procédure endovasculaire, une laparotomie exploratrice sera le plus souvent nécessaire afin d’explorer la viabilité intestinale et de réaliser une résection partielle si nécessaire.
Ischémie mésentérique chronique
L’atteinte athéromateuse chronique mésentérique est souvent sous-diagnostiquée. Les douleurs abdominales postprandiales sont évocatrices, associées à une perte de poids. L’examen de première ligne est l’écho-Doppler artériel.
En cas de sténose symptomatique, une revascularisation doit être proposée sans délai et le choix du mode de revascularisation sera discuté en équipe multidisciplinaire. En cas de découverte d’une sténose chez un patient asymptomatique, il n’y a aucune d’indication à une revascularisation.
Atteinte rénale
L’exploration des artères rénales est préférentiellement réalisée par échographie-Doppler. L’ARM (angiographie par résonance magnétique) ou le scanner sont également possibles. Du fait de l’absence d’efficacité de la revascularisation rénale sur le pronostic cardiovasculaire, celle-ci n’est plus indiquée en cas de sténose de plus de 60%. Le traitement médical reste la règle, incluant la prescription d’IEC ou d’ARA2 sous surveillance rapprochée de la fonction rénale.
La revascularisation rénale, par voie endovasculaire, ne reste donc indiquée que dans des situations particulières, avec cependant un faible niveau de preuve:
• œdème aigu pulmonaire flash ou insuffisance cardiaque congestive
• insuffisance rénale oligo-anurique
La dysplasie fibro-musculaire présente un cas spécifique d’hypertension réno-vasculaire. Dans ce contexte, une revascularisation rénale par angioplastie au ballon seule peut être proposée en première ligne chez un patient symptomatique avec signe de souffrance d’organe.
Évaluation des atteintes polyvasculaires
En cas de pathologie vasculaire périphérique symptomatique, la présence d’une autre atteinte de localisation athéromateuse symptomatique est très fréquente.
A gravité égale de l’atteinte vasculaire périphérique, l’atteinte polyvasculaire aggrave de façon significative le pronostic de ces patients. Un dépistage systématique des localisations athéromateuses à chaque étage n’est cependant pas recommandé en l’absence de symptômes. En effet, la découverte de lésions asymptomatiques ne modifiera pas la prise en charge globale, qui nécessite un traitement médical optimal. L’examen clinique par un interrogatoire méticuleux, la recherche de souffle, de l’abolition de pouls, reste la pierre angulaire du dépistage, devant orienter la prescription des examens complémentaires.
Dans le cas du bilan préopératoire du pontage coronarien, le dépistage des sténoses carotidiennes n’est recommandé qu’en cas d’AVC ou d’AIT récent. Il peut être réalisé si âge > 70 ans, en cas de souffle carotidien ou d’atteinte polyvasculaire connue, mais pas de manière systématique chez tout patient adressé avant chirurgie.
La revascularisation carotidienne avant pontage coronarien ne sera réalisée qu’en cas d’atteinte bilatérale sévère (c’est à dire de sténoses >70% bilatérales ou soit 1 sténose >70% avec une occlusion controlatérale). Inversement, un dépistage de la coronaropathie par coronarographie en cas de sténose carotidienne ne sera systématique qu’en cas de chirurgie carotidienne programmée (classe IIb).
Évaluation cardiaque en cas de maladie artérielle périphérique
Les comorbidités cardiaques sont fréquentes en cas de maladies artérielles périphériques. La fibrillation auriculaire et l’insuffisance cardiaque sont au premier rang, en plus de la pathologie coronarienne.
Pour ces raisons, un dépistage de l’insuffisance cardiaque par dosage du BNP et / ou réalisation d’une échographie transthoracique a fait l’objet d’une nouvelle recommandation en cas de pathologie artérielle symptomatique.
En cas de fibrillation auriculaire associée à une AMI, l’anticoagulation est bien sûr recommandée en cas de score de CHA2DS2-VASC ≥2 (classe I) mais peut également être proposée (classe IIa) quel que soit le score, chez un patient avec AMI symptomatique.
Réciproquement, le dépistage de l’AMI par réalisation de l’IPS est recommandé en cas d’insuffisance cardiaque symptomatique ou de pathologie coronarienne.
Conclusion
Ces recommandations ont l’avantage de regrouper de manière synthétique les conduites à tenir dans les cas de maladies artérielles périphériques. Elles apportent une vision globale de la prise en charge du patient polyvasculaire, en insistant sur le traitement médical optimal sans oublier l’évaluation des comorbidités, notamment cardiaques. Le choix, souvent complexe, d’une procédure de revascularisation adaptée doit reposer sur des équipes vasculaires multidisciplinaires.
Guillaume Goudot, Emmanuel Messas
Service de médecine vasculaire, Hôpital Européen Georges Pompidou, Paris
L’auteur déclare ne pas avoir de lien d’intérêt avec le sujet traité.
RÉFÉRENCES
1. Aboyans V, Ricco J-B, Bartelink M-LEL, et al. 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS). Eur Heart J Published Online First: 26 August 2017. doi:10.1093/eurheartj/ehx095
2. Mills JL, Conte MS, Armstrong DG, et al. The Society for Vascular Surgery Lower Extremity Threatened Limb Classifi cation System: risk stratifi cation based on wound, ischemia, and foot infection (WIfI). J Vasc Surg 2014;59:220-34-2. doi:10.1016/j.jvs.2013.08.003
3. Anand SS, Bosch J, Eikelboom JW, et al. Rivaroxaban with or without aspirin in patients with stable peripheral or carotid artery disease: an international, randomised, double-blind, placebo-controlled trial. Lancet Published Online First: 10 November 2017. doi:10.1016/S0140-6736(17)32409-1
