
Intérêt d’évaluer la rigidité artérielle au-delà de la pression artérielle en elle-même
La rigidité artérielle se mesure facilement et peut apporter beaucoup au clinicien en termes de compréhension de la physiopathologie, du système artériel et de valeur prédictive des complications cardiovasculaires. Il existe une idée trop souvent répandue selon laquelle, la valeur de la rigidité artérielle étant liée à la pression artérielle, il suffit de mesurer la pression artérielle pour estimer le risque de complications cardiovasculaires et adapter le traitement. L’objectif de cet article est de démontrer que ce n’est pas le cas et que la rigidité artérielle a un intérêt au-delà de la pression artérielle en termes de valeur prédictive des complications cardiovasculaires et de stratégie thérapeutique. Après un bref rappel de la physiologie de la rigidité artérielle et des méthodes de mesure, seront discutés le rôle de la rigidité artérielle dans la physiopathologie de l’hypertension artérielle (HTA), du diabète et de l’insuffisance rénale ; la valeur prédictive de la rigidité artérielle pour les complications cardiovasculaires indépendamment de la pression artérielle et des facteurs de risque cardiovasculaires classiques ; la réduction pression-indépendante de la rigidité artérielle ; et la possibilité que la rigidité artérielle soit un critère de substitution de la pression artérielle dans le traitement de l’HTA.
Introduction
La rigidité artérielle se mesure facilement et peut apporter beaucoup au clinicien en termes de compréhension de la physiopathologie du système artériel et de valeur prédictive des complications cardiovasculaires (CV). C’est par ailleurs un bon outil d’éducation thérapeutique chez l’hypertendu et d’aide à l’observance médicamenteuse. Cependant, la mesure de la rigidité artérielle est encore insuffisamment utilisée en pratique clinique, malgré les recommandations des Sociétés Européennes d’Hypertension Artérielle (ESH) et de Cardiologie (ESC)1 . Parmi les raisons de cette réticence, il y a l’idée trop souvent répandue que la valeur de la rigidité artérielle étant liée à la pression artérielle (PA), il suffit de mesurer la PA pour estimer le risque de complications CV et adapter le traitement chez l’hypertendu, et qu’il suffit de baisser la PA pour diminuer la rigidité artérielle et réduire le risque d’évènements CV.
L’objectif de cet article est de démontrer que ce n’est pas le cas et que la rigidité artérielle a un intérêt au-delà de la PA en termes de valeur prédictive des complications CV et de stratégie thérapeutique. Après un bref rappel de la physiologie de la rigidité artérielle et des méthodes de mesure, seront discutés le rôle de la rigidité artérielle dans la physiopathologie de l’hypertension artérielle (HTA), du diabète et de l’insuffisance rénale ; la valeur prédictive de la rigidité artérielle pour les complications CV indépendamment de la PA et des facteurs de risque CV classiques ; la réduction pression-indépendante de la rigidité artérielle ; et la possibilité que la rigidité artérielle soit un critère de substitution de la PA dans le traitement de l’HTA.
Physiologie de la rigidité artérielle
« Rigidité artérielle » est un terme général qui représente la capacité qu’ont tous les gros troncs artériels à se distendre lors du passage de l’onde de pression systolique, à emmagasiner ainsi l’énergie développée, et à la restituer lors de la diastole au travers d’un mécanisme passif de retour à un calibre pré-systolique. Ce mécanisme est lié à la structure de la média, riche en lamelles élastiques qui jouent un rôle passif et en cellules musculaires lisses vasculaires qui jouent un rôle actif 2 . Au plan fonctionnel, l’intérêt majeur de la rigidité artérielle est représenté par la capacité qu’ont les grosses artères proximales au cœur d’atténuer la pulsatilité de la pression générée par la contraction cardiaque intermittente et de transformer un débit pulsatile dans l’aorte ascendante en un débit quasi continu au niveau des artérioles. Faute de quoi, le débit de perfusion des organes cibles (rein, cerveau) devient hyperpulsatile avec pour conséquence un remodelage artériolaire hypertrophique interne, c’est-à-dire une paroi plus épaisse et un calibre réduit, dont on connaît les conséquences sur les fonctions rénales et cognitives qui s’altèrent. Mais aussi, une aorte rigide conduit à générer des ondes de pression réfléchies qui retournent au cœur, se superposent aux ondes incidentes et augmentent ainsi la PA systolique, donc la post-charge, génèrent de l’hypertrophie ventriculaire gauche et diminuent le remplissage coronaire.
Mesure de la rigidité artérielle
Le « Gold Standard » de la mesure de la rigidité artérielle est la vitesse de propagation de l’onde de pouls carotido-fémorale (VOPcf) le long de l’aorte thoracoabdominale3 . Cela consiste à enregistrer l’onde de pouls au niveau de la carotide commune et de l’artère fémorale commune, à calculer le délai entre les pieds des ondes de pression, et à diviser la longueur parcourue par ce délai. La vitesse est donnée en mètres par seconde (m/s). La distance parcourue par l’onde de pression est estimée par la distance carotido-fémorale affectée d’un coefficient pour tenir compte que l’éjection se fait dans un sens vers la carotide et dans un autre vers l’aorte descendante. On peut remplacer la mesure de l’onde de pression (qui utilise des mécanocapteurs) par la mesure du flux par Doppler. Les appareils de mesure les plus populaires sont le Sphygmocor (Atcor®) et le Complior (Alam Medical®). La mesure de la rigidité artérielle est assez simple, une fois acquises les bonnes pratiques. Elle est surtout robuste, c’est-à-dire que les valeurs sont très reproductibles. En pratique clinique, la mesure dure environ 20 minutes, en comptant le temps de repos allongé de 10 minutes qui précède la mesure. Des appareils plus simples et d’un moindre coût ont été mis au point, comme le pOpmètre (Axelife®). A côté de ces mesures directes en deux points, ont été développées des méthodes indirectes en un seul point de mesure, au niveau de l’artère humérale, qui enregistrent la courbe de pression artérielle sur plusieurs cycles et estiment la rigidité artérielle, ou qui la dérivent à partir de l’intervalle QKd. Les recommandations de l’ESH-ESC 2013 et 2018 fixent à 10 m/s le seuil au-delà duquel la VOPcf est anormalement élevée.
Physiopathologie de la rigidité artérielle : concept d’EVA
La rigidité artérielle augmente chez l’hypertendu, à la fois en réponse à l’augmentation de la pression intra-artérielle qui met en tension les fibres les plus rigides de la paroi artérielle, mais aussi en réponse aux modifications structurales, dites de « remodelage chronique », qui surviennent au long cours pour adapter la paroi à l’excès de pression. S’y ajoute un changement de phénotype de nombreux éléments de la paroi artérielle, comme les cellules musculaires lisses vasculaires, les composants de la matrice extracellulaire et les éléments impliqués dans la relation cellulematrice, qui jouent un grand rôle chez le diabétique et l’insuffisant rénal chronique.
En pratique clinique, les déterminants majeurs d’une augmentation de la rigidité artérielle sont l’âge, le sexe, la PA (PAS et PAM), le diabète, l’index de masse corporelle, le tabagisme, la sédentarité, en bref tous les facteurs de risque CV classiques. Mais, et c’est là tout l’intérêt de la mesure de la rigidité artérielle, à même facteurs de risque CV (en nombre et en intensité, donc en score) certains sujets ont une rigidité très élevée alors que d’autres semblent protégés et ont une rigidité artérielle beaucoup moins élevée qu’attendu (Figure 1).

Les premiers rentrent dans la catégorie des EVA (Early Vascular Aging – Vieillissement artériel précoce ou accéléré), tandis que les seconds peuvent être qualifiés de SUPERNOVA (SUPERNOrmal Vascular Aging – âge vasculaire supernormal). Nous avons popularisé ces concepts lors des 10 dernières années 4-6. On comprend donc que l’intérêt de mesurer la rigidité artérielle est double. D’une part, la rigidité est un intégrateur de toutes les agressions de la paroi artérielle qui surviennent au cours du temps, qu’elles soient mesurables (facteurs de risque CV classiques) ou non mesurables (stress oxydant, inflammation chronique de bas grade, epigénétique, etc…). D’autre part, la rigidité artérielle est un révélateur de la capacité des individus à amplifier ces agressions (EVA)5 ou au contraire à s’en protéger (SUPERNOVA)5,6. Conclusion : calculer un score de risque CV à un instant « t », c’est bien, mais cela ne prend en compte ni l’historique des agressions de la paroi (donc leurs fluctuations dans le temps), ni la susceptibilité de l’individu à les amplifier ou à s’en protéger. On peut raisonner de la même manière vis-à-vis de la PA. La mesure de la rigidité artérielle intègre les dommages subis en réponse à l’élévation de la PA et ses fluctuations tandis que quelques mesures de la PA, même répétées sur 24h avec la MAPA, ne rendent pas compte de la charge tensionnelle cumulée sur des années.
Valeur prédictive indépendante de la pression artérielle
Compte-tenu de ce qui a été développé plus haut, il n’est pas étonnant que de nombreuses études longitudinales aient démontré que la mesure de la rigidité artérielle (le plus souvent VOPcf) ait une bonne valeur prédictive pour les complications CV audelà de la PA ou des scores de risque CV (Euroscore ou score de Framingham), c’est-à-dire que sa valeur prédictive reste significative après ajustement sur ces paramètres. Ceci a été retrouvé dans des populations très diverses (normotendus, hypertendus, diabétiques, insuffisants rénaux, coronariens, sujets âgés…) et pour des complications et des événements variés (décès CV, mortalité totale, infarctus, pontage, angioplastie, AVC, récupération fonctionnelle après AVC, survenue d’une hypertension, nécessité d’une dialyse, …). Dix ans après les études pionnières 7 , deux méta-analyses 8 , dont une en données individuelles, ont quantifié le sur-risque : + 15% de mortalité CV pour toute augmentation de VOPcf de 1 m/s, soit + 45% pour 3 m/s ; ainsi qu’un risque multiplié par 2,5 chez l’hypertendu et 2,8 chez le dialysé quand la VOPcf est supérieure à la médiane par rapport au risque observé quand la VOPcf est inférieure. Ces résultats sont tous indépendants de la PA.
Réduction pression indépendante de la rigidité artérielle
On a vu plus haut que l’augmentation de la rigidité artérielle était prédictive d’une augmentation du risque CV et que cette relation était en partie indépendante de la PA. L’application de ces résultats à la pratique clinique est qu’une diminution de la rigidité artérielle devrait s’accompagner d’une réduction des complications CV indépendamment de la baisse de la PA. Il faudrait pour cela qu’il soit possible d’améliorer la rigidité artérielle au travers de mécanismes non pression-dépendants. Des mécanismes cellulaires et moléculaires ont été évoqués, comme le remodelage de la paroi artérielle ciblé sur la connexion entre éléments distensibles et éléments fibreux et rigides. D’autre part, il existe de nombreuses évidences pharmacologiques que certaines classes d’antihypertenseurs sont capables de diminuer la rigidité artérielle au-delà de la baisse de la PA lorsque leur administration est prolongée (au moins 3 mois) et réalisée aux plus fortes doses. C’est le cas pour les IEC tels que le perindopril ou le trandolapril, les ARA2 tels que le valsartan et l’olmesartan, et les anti-aldostérone (spironolactone). Par ailleurs, une méta-analyse9 et plusieurs revues ont montré que les bloqueurs du système rénine-angiotensine-aldostérone et les antagonistes calciques sont plus efficaces que les bêtabloquants et les diurétiques pour réduire la rigidité artérielle indépendamment de la baisse de la PA.
La rigidité artérielle comme critère de substitution
Baisser la PA chez l’hypertendu, c’est garantir une réduction du risque CV. Parce que la PA est considérée comme un critère de substitution. C’est-à-dire qu’il suffit de mesurer la PA en pratique clinique pour s’assurer qu’on fait œuvre utile chez l’hypertendu en prescrivant des antihypertenseurs. Mais aussi parce que de très nombreux essais cliniques ont montré que les médicaments antihypertenseurs baissent la PA et diminuent les évènements CV, et que le premier entraîne le second. En d’autres termes, la mesure de la PA se substitue à l’évaluation des complications qui nécessiterait un long suivi sur un très grand nombre de patients. Très peu de mesures de l’atteinte des organes cibles ont obtenu la qualité de « critère de substitution » : seuls l’HVG grâce à l’étude LIFE et la micro-albuminurie grâce aux études LIFE, RENAAL, IDNT et ONTARGET peuvent être qualifiés de critères de substitution. Mais pas encore la rigidité artérielle.
L’étude SPARTE10 est pour l’instant la seule étude qui ait cherché à répondre à la question suivante : en mesurant régulièrement la rigidité artérielle et en choisissant les médicaments antihypertenseurs les plus adaptés à la normaliser, est-on plus efficace qu’en mesurant seulement la PA ? L’étude SPARTE, menée en France de 2013 à 2020, randomisée en groupes parallèles, a suivi 536 hypertendus pendant 4 ans, en les traitant soit selon les recommandations internationales ESH-ESC (groupe conventionnel), soit en ajustant le traitement aux mesures de la rigidité artérielle de manière à baisser la VOPcf en dessous de 10 m/s (groupe VOP) (Figure 2).
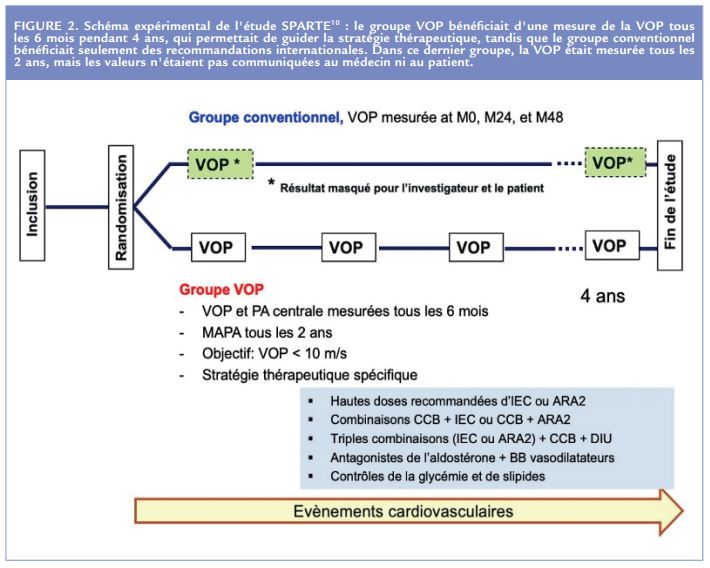
Dans ce dernier groupe, il était recommandé de privilégier les combinaisons d’antagonistes calciques et d’IEC (ou ARA2) aux plus fortes doses recommandées, comme cela a été discuté plus haut. Une telle intensification thérapeutique a bien été observée au cours de l’étude. S’y associait une réduction de la PAS et de la PAD, en consultation et à la MAPA, et une baisse de la VOPcf par rapport au groupe conventionnel. Environ la moitié de la baisse de la VOP était liée à la baisse de la PA et l’autre moitié aux modifications structurales et fonctionnelles survenant au long cours en réponse à la stratégie thérapeutique décrite plus haut. Les évènements CV ont été réduits de 26% dans le groupe VOP, mais l’intervalle de confiance de la réduction fut trop large pour que cette baisse soit significative. L’étude SPARTE10, étude académique, peut donc être considérée non seulement comme une tentative de preuve de concept que la rigidité artérielle est bien un critère de substitution, mais aussi comme une étude de faisabilité incitant d’autres groupes de recherche, en particulier les industriels du médicament qui disposent de gros moyens financiers, à la répliquer dans une population plus grande et peut-être plus ciblée (patients à très haut risque CV).
Par ailleurs, c’est la première fois que la rigidité artérielle est mesurée tous les 6 mois pendant une durée aussi prolongée (4 ans) sur un aussi grand nombre de patients. Cela a permis de montrer qu’une stratégie thérapeutique adaptée peut empêcher le vieillissement artériel, car la VOP est restée stable dans le groupe VOP alors qu’elle augmentait dans le groupe conventionnel.
Enfin, l’étude SPARTE démontre qu’il a été possible de baisser la PA chez des patients dont l’HTA était considérée pour la majorité d’entre eux comme contrôlée, puisqu’ils avaient en moyenne 134/77 mmHg de PAS/PAD à l’inclusion et que les deux tiers d’entre eux avaient une PA inférieure à 140/90 mmHg. En revanche, l’absence de baisse de PA dans le groupe conventionnel montre qu’il est insuffisant de cibler un intervalle de 130-139/80-85 mmHg selon les recommandations, et que c’est le rôle éducatif, pour le patient et le médecin, des mesures répétées de rigidité artérielle qui a permis de baisser la PA dans le groupe VOP.
Conclusion
La rigidité artérielle se mesure facilement. Sa popularité en pratique clinique est insuffisante en regard de l’abondance des preuves scientifiques en faveur de sa valeur prédictive des complications cardiovasculaires, qui se révèle indépendante de la pression artérielle. La mesure de la rigidité artérielle permet de guider la stratégie thérapeutique. C’est aussi un bon outil d’éducation thérapeutique pour une meilleure observance. Après un traitement de plusieurs mois, la réduction de la rigidité artérielle est pour moitié liée à la baisse de la PA et pour moitié aux modifications structurales et fonctionnelles liées au remodelage induit par certaines classes pharmacologiques. Les plus efficaces sont les IEC et les ARA2 aux plus fortes posologies recommandées, prescrits en association avec les antagonistes calciques. Si la PA est un critère de substitution aux complications CV, la rigidité artérielle ne remplit pour l’instant pas les conditions d’un tel critère de substitution.
Stéphane Laurent Université de Paris et INSERM U 970, Paris
RÉFÉRENCES
- Williams B, Mancia G, Spiering W, et al. Authors/Task Force Members: 2018 ESC/ESH Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension. Eur Heart J 2018 ; 39:3021-3104
- Lacolley P, Regnault V, Segers P, Laurent S. Vascular Smooth Muscle Cell and Arterial Stiffening: Relevance in Development, Ageing and Disease. Phys Rev 2017;97:1555-1617
- Laurent S, Cockcroft J, Van Bortel L, Boutouyrie P, Giannattasio C, Hayoz D, Pannier B, Vlachopoulos C, Wilkinson I, Struijker-Boudier H; European Network for Non-invasive Investigation of Large Arteries. Expert consensus document on arterial stiffness: methodological issues and clinical applications. Eur Heart J. 2006 ;27:2588-2605
- Nilsson P, Boutouyrie P, Laurent S. Vascular aging: A tale of EVA and ADAM in cardiovascular risk assessment and prevention. Hypertension 2009; 54:3-10
- Laurent S, Boutouyrie P, Cunha PG, Lacolley P, Nilsson PM. Concept of Extremes in Vascular Aging. Hypertension. 2019;74:218-228.
- Bruno RM, Nilsson PM, Engsrtom G, Wadstrom B, Empana JP, Boutouyrie P, Laurent S. Early and SUPERNOrmal Vascular Aging (EVA and SUPERNOVA): clinical characteristics and cardiovascular events. Hypertension 2020;76:1616- 1624.
- Laurent S, Boutouyrie P, Asmar R, Gautier I, Laloux B, Guize L, Ducimetiere P, Benetos A. Aortic stiffness is an independent predictor of all-cause and cardiovascular mortality in hypertensive patients. Hypertension, 2001, 37: 1236-1241.
- Vlachopoulos C, Aznaouridis K, Stefanadis C. Prediction of cardiovascular events and all-cause mortality with arterial stiffness: a systematic review and meta-analysis. J Am Coll Cardiol. 2010; 55:1318-27
- Ong KT, Delerme S, Pannier B, Safar M, Benetos A, Laurent S, Boutouyrie P. Aortic stiffness is reduced beyond blood pressure lowering by short- and long-term antihypertensive treatment: a meta-analysis of individual data in 294 patients. J Hypertens 2011;29:1034-1042
- Laurent S, Chatellier G, Azizi M et al. The SPARTE Study: normalisation of arterial stiffness and cardiovascular events in patients with hypertension at medium to very high risk. Hypertension 2021, sous presse
Cordiam N°41 – AOÛT – SEPTEMBRE 2021
