
Rationnel de l’étude
Les épisodes d’insuffisance cardiaque aiguë (ICA), de novo ou émaillant l’évolution d’une insuffisance cardiaque (IC) chronique, sont associés à des symptômes limitant les capacités à l’effort.¹ Au même titre que la diminution des hospitalisations et de la mortalité cardiovasculaire, l’amélioration de la qualité de vie et des capacités à l’exercice est un objectif central dans la prise en charge de l’IC.
Les inhibiteurs des sodium-glucose transporteurs de type 2 (iSGLT2 ou gliflozines) ont prouvé leur efficacité pour réduire la mortalité cardiovasculaire et les ré-hospitalisations pour ICA en cas d’IC à FEVG altérée² ³ ou préservée.4
Plus récemment, l’étude EMPULSE a montré le bénéfice clinique des gliflozines sur la mortalité toutes causes en cas d’introduction après un épisode d’ICA. Néanmoins l’effet sur les symptômes, les capacités à l’effort et la qualité de vie ont été moins étudiés.5
Design de l’étude
L’étude EMPULSE5 est une étude multicentrique (118 centres Européens, Nord-Américains et Asiatiques) ayant inclus des patients en ICA (de novo ou décompensation d’IC chronique connue, indépendamment de la FEVG et du statut diabétique).
Les patients étaient randomisés entre empagliflozine (10 mg par jour) versus placebo pour une durée de 90 jours (Figure 1).
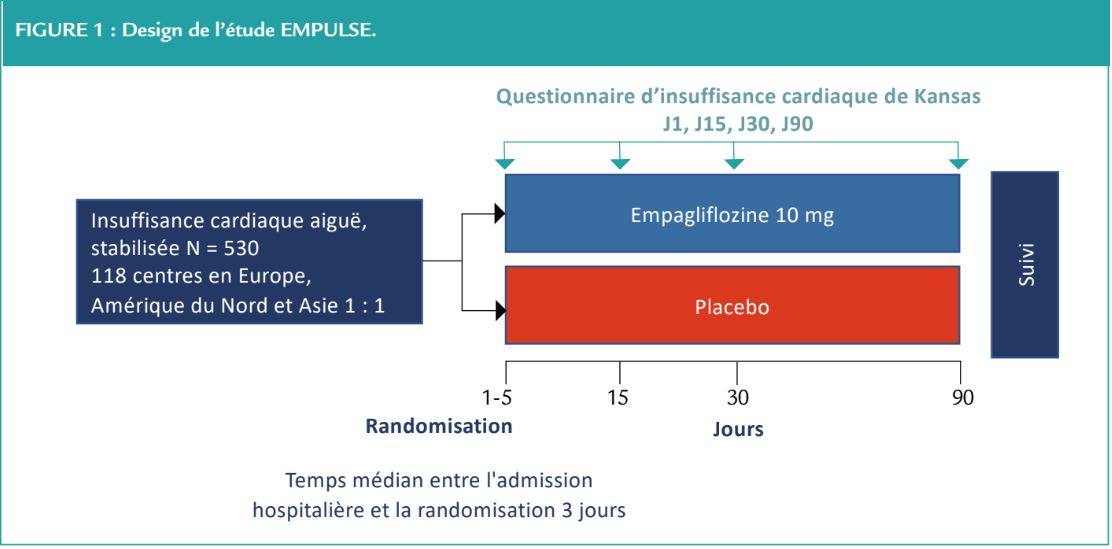
Dans cette seconde analyse, le critère de jugement principal composite était les bénéfices cliniques à 90 jours, défini par : le délai jusqu’au décès toute cause, le nombre d’hospitalisation pour ICA et enfin le délai jusqu’au premier épisode d’IC. Une analyse post-hoc a stratifié (en tertile) la population selon le degré de symptomatologie (évalué par le Kansas City Cardio- myopathy Questionnaire [KCCQ] score) à l’inclusion.
Les critères de jugement secondaires étaient l’amélioration des paramètres suivants (entre l’inclusion et J90) : les symptômes (évalués par le KCCQ Total Symptom Score [TSS]), la limitation d’activité physique (évaluée par le KCCQ Physical Limitation Scale [PLS]), la qualité de vie (évaluée par le KCCQ Quality of Life Social Limitations Scales [QoL]), le KCCQ clinique (TSS et
CSS) et le KCCQ total (TSS, PLS et QoL).
Principaux résultats
Au total, 530 patients ont été randomisés en 1:1 (n=265 dans chaque bras). L’âge moyen était de 68,5 13,3 ans avec 34% de femmes. La FEVG était ≤ 40% dans 67% des cas et les patients étaient en classe fonctionnelle NYHA III-IV dans 62% des cas. A l’inclusion, le KCCQ-TSS score était de 40,8 24,0. Quant au NTproBNP, sa médiane était de 3 245,8 (1 735,4 – 6 104,3) pg/mL. L’IC était majoritairement de cause non ischémique (71,9%). On pourra noter, sans pour autant connaitre la répartition de la FEVG parmi les patients, que les bétabloquants étaient présents chez 79% des patients, les IEC/ARA2 ou ARNI dans 70% des cas et enfin les ARM dans 52% des cas à l’inclusion.
Concernant le critère de jugement principal, il existait une amélioration significative du critère de jugement principal en faveur de l’empagliflozine en considérant l’ensemble de la population traitée indépendamment du niveau de KCCQ score à l’inclusion. (Figure 2).
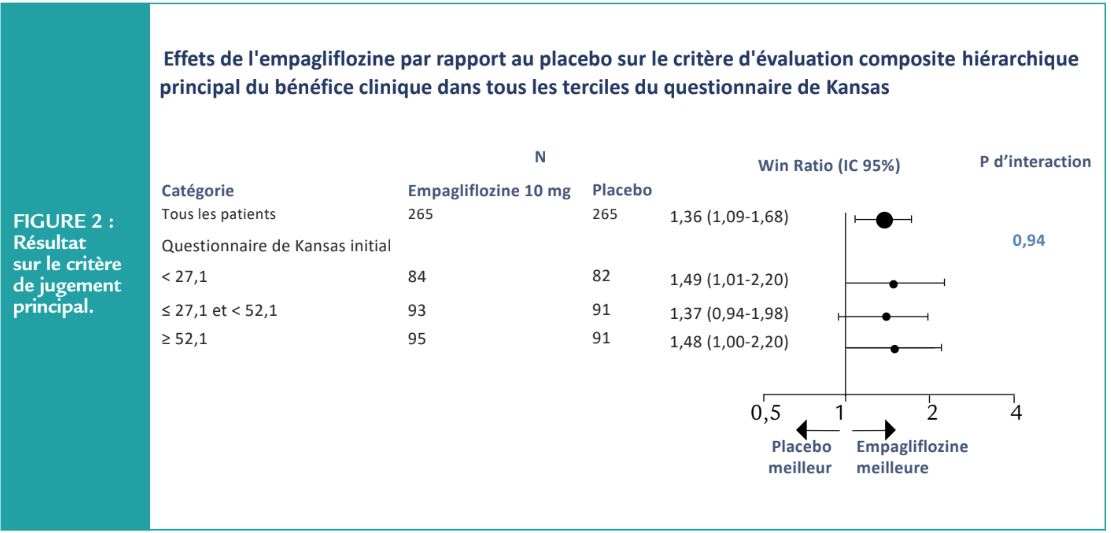
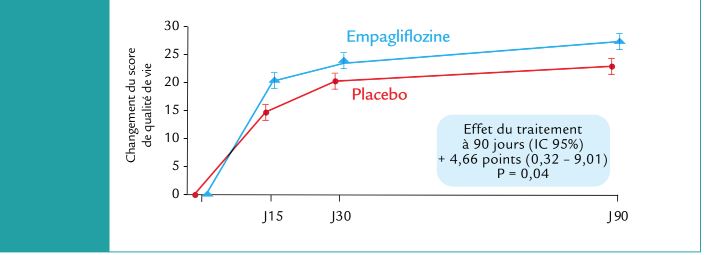
Concernant les critères de jugement secondaires, il existait une amélioration significativement plus importante du KCCQ-TSS score, du KCCQ-QoL, du KCCQ clinique et total dans le groupe empagliflozine (Figure 3). Ces bénéfices étaient visibles dès J15 et persistaient à J90.
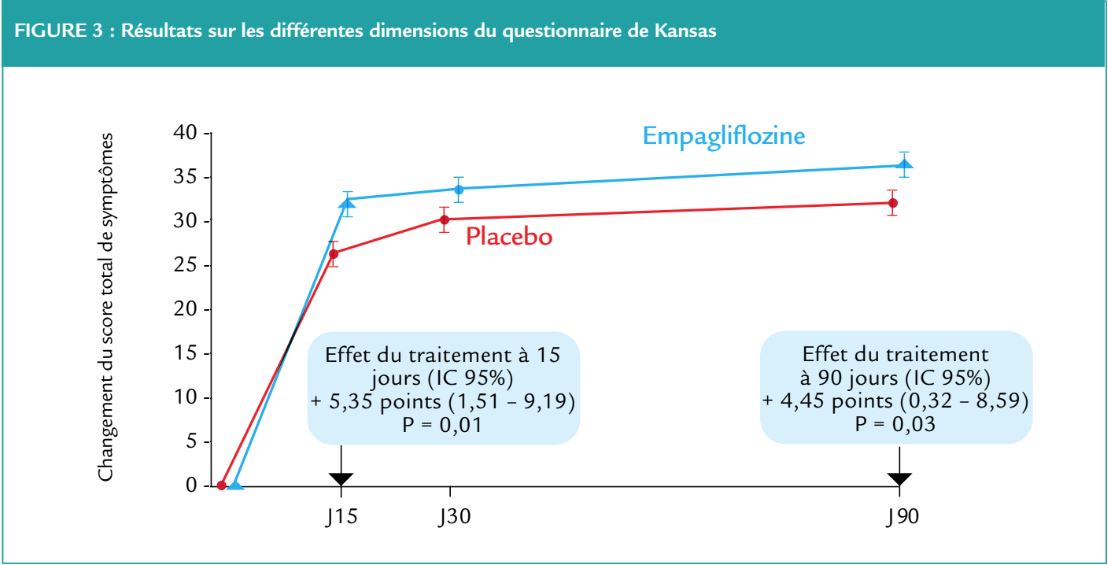
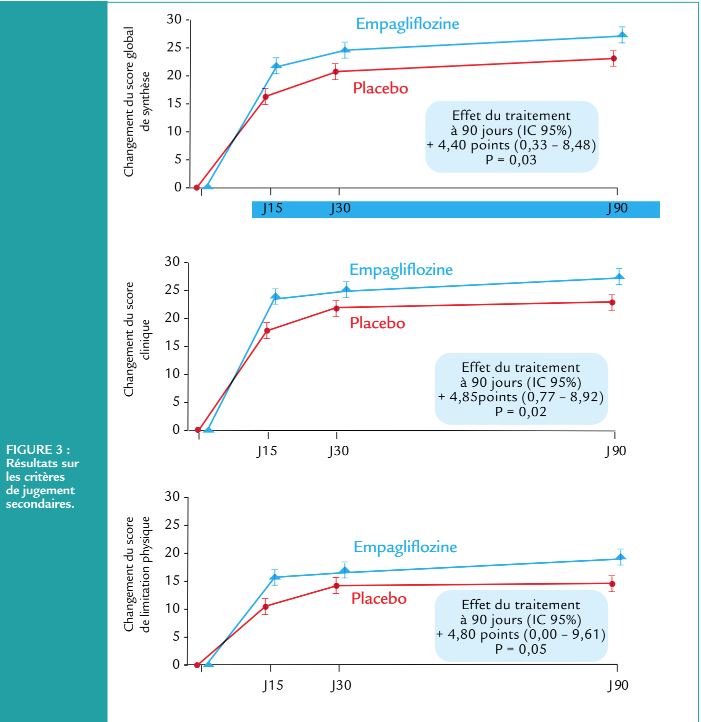
Conclusion et mise
en perspective
L’initiation d’empagliflozine chez les patients hospitalisés pour ICA, quels que soient la FEVG et le statut diabétique, permet une amélioration significative des symptômes, de la qualité de vie ainsi qu’une diminution des limitations à l’effort dès 15 jours de traitement.
Cette analyse d’EMPULSE conforte la place des iSGLT2 dans l’arsenal thérapeutique de l’IC. Elle souligne aussi l’intérêt de cette molécule en phase précoce post-décompensation et même chez des patients avec une IC de novo (qui n’avaient pas été inclus jusqu’ici).
QUE RETENIR POUR MA PRATIQUE QUOTIDIENNE ?
L’étude EMPULSE avait déjà montré le bénéfice des gliflozines en cas d’hospitalisation pour IC aigue sur un critère composite comprenant entre autres, décès toute cause ou hospitalisation pour IC.
- Cette sous analyse de l’étude EMPULSE montre que l’empagliflozine, initiée lors d’épisode d’IC aiguë (quels que soient la FEVG et le statut diabétique), permet une réduction significative des symptômes et une amélioration des capacités à l’effort et de la qualité de vie des patients.
- Cet effet est significatif dès J15 et persiste jusqu’à 3 mois.
- Cela renforce l’intérêt de cette molécule en phase précoce d’IC aigue pour améliorer la qualité de vie et éviter des ré-hospitalisations précoces pour IC.
CORDIAM, Supplément au n°45, Mars-Avril 2022
Charles Fauvel,
Rouen
Références
- McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021 Aug 27;ehab368.
- McMurray JJV, Solomon SD, Inzucchi SE, Køber L, Kosiborod MN, Martinez FA, et al. Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction. N Engl J Med. 2019 Nov 21;381(21):1995–2008.
- Packer M, Anker SD, Butler J, Filippatos G, Pocock SJ, Carson P, et al. Cardiovascular and Renal Outcomes with Empagliflozin in Heart Failure. N Engl J Med. 2020 Oct 8;383(15):1413–24.
- Anker SD, Butler J, Filippatos G, Ferreira JP, Bocchi E, Böhm M, et al. Empagliflozin in Heart Failure with a Preserved Ejection Fraction. N Engl J Med. 2021 Aug 27;
- Voors AA, Angermann CE, Teerlink JR, Collins SP, Kosiborod M, Biegus J, et al. The SGLT2 inhibitor empagliflozin in patients hospitalized for acute heart failure: a multinational randomized trial. Nat Med.
