
Approche centrée sur le patient, particularités pharmacologiques, durabilité d’action, risques cardiovasculaires, tels sont les thèmes abordés lors de cette session consacrée à la prise en charge du diabète de type 2 et plus particulièrement au traitement par les inhibiteurs de la DPP4.
Dimension patient pour une décision médicale partagée
L’importance de développer une approche centrée sur le patient dans le diabète de type 2 a été rappelée en 2012 par l’American Diabetes Association (ADA) et l’European Association for the Study of Diabetes (EASD)(1,2), et est reconnue par la Société Francophone du Diabète. Elle a aussi fait l’objet en 2013 d’un état des lieux par la Haute Autorité de Santé(3). Cette notion ne doit pas être confondue, comme on le fait souvent, avec une approche individualisée selon le phénotype des patients, qui prendra par exemple en compte des paramètres comme le risque d’hypoglycémie, le taux d’HbA1c, la présence de complications pour éviter des prescriptions contre-indiquées… Dans ce dernier cas, il s’agit seulement d’une approche centrée sur la maladie, étape certes indispensable mais non suffisante. L’approche centrée sur le malade va plus loin et définit, comme le rappellent les experts de l’ADA et de l’EASD, une démarche « destinée à apporter un soin qui soit respectueux du patient, adapté à ses préférences individuelles, ses besoins et ses valeurs, et qui fasse en sorte que celles-ci guident l’ensemble des décisions cliniques ». Ces spécialistes soulignent que cette approche, « qui devrait être le principe organisateur sous-jacent des soins de santé pour les personnes ayant une maladie chronique, est particulièrement appropriée dans le diabète de type 2, étant donné nos incertitudes en termes de choix ou de séquence thérapeutique ». Ils proposent un tableau où toutes les options thérapeutiques (sulfamides, glinides, glitazones, inhibiteurs de l’alpha-glucosidase, inhibiteurs de la DPP4 et de la SGLT2, agonistes du récepteur du GLP1, insuline) peuvent être utilisées en bithérapie avec la metformine, qui continue de faire consensus en monothérapie. Les avantages et inconvénients de chaque possibilité thérapeutique sont détaillés de façon à guider le patient dans ses choix.
Une approche compatible avec l’EBM
Cette approche centrée sur le patient n’est, en rien, incompatible avec l’Evidence-based-medicine (EBM). A l’origine conçue pour éclairer les médecins dans leurs prises de décision, l’EBM est souvent devenue une méthode de gestion des risques contribuant à la standardisation de la pratique médicale et à la déshumanisation de la relation entre soigné et soignant. Pourtant, pour ses initiateurs, elle devait prendre en compte, outre les données des essais randomisés, l’expertise du clinicien et l’implication du patient.
Une méta-analyse de 115 études randomisées contrôlées, ayant impliqué 34 444 participants, laisse penser que la décision médicale partagée se traduit par une perception plus juste par les patients des risques, des malades plus à l’aise par rapport aux décisions prises(4). Des spécialistes comme la Britannique, Angela Coulter, considèrent aussi qu’avec cette approche, les patients « adhèrent mieux aux traitements, rencontrent moins d’effets indésirables, ont moins recours à des soins coûteux ». Dans tous les cas, le clinicien devra, pour éclairer les décisions de son patient diabétique, l’informer sur la maladie, les examens à réaliser, les bénéfices et risques des différentes stratégies thérapeutiques. Il pourra s’aider, dans ce but, de pictographes, comme ceux développés pour expliquer de façon imagée la réduction du risque cardiovasculaire sous statine, car certains malades éprouvent des difficultés à comprendre les données statistiques. Des outils existent pour aider les patients à obtenir, en particulier sur internet, des informations neutres sur leur maladie et ses suites, avec ou sans traitement, ainsi que pour clarifier ce qui est important pour eux en fonction de leurs valeurs. Malheureusement, ils sont encore peu répandus en France et dans le diabète.
D’après la communication de : Alfred Penfornis, Centre Hospitalier Sud Francilien, Corbeil-Essonnes.
Alfred Penformis
Dimension pharmacologique
La réponse incrétine est atténuée dans le diabète de type 2 et s’accompagne d’un abaissement du taux de GLP1. Les travaux précliniques suggèrent que ce peptide est doté d’effets cardiovasculaires bénéfiques, directs ou indirects (et alors médiés par une action centrale ou rénale) : effet vasodilatateur, action inotrope positive, amélioration de la fonction ventriculaire gauche après infarctus du myocarde. Les deux grandes stratégies thérapeutiques utilisées pour restaurer les taux de GLP1 sont d’utiliser des analogues de son récepteur, ou de limiter sa dégradation endogène en inhibant la dipeptidyl-peptidase 4 (DPP4). Nouvel inhibiteur de la DPP4, l’alogliptine se caractérise par des propriétés pharmacologiques : sélectivité d’action vis-à-vis de la DPP4, absence d’interaction avec la voie du cytochrome P450, longue demi-vie (12 à 21 heures), biodisponibilité orale de 100% limitant les variations de concentrations plasmatiques. Son taux de fixation aux protéines plasmatiques est relativement faible (20%) et comme pour plupart des médicaments de cette classe, son élimination est principalement rénale (Figure 2).
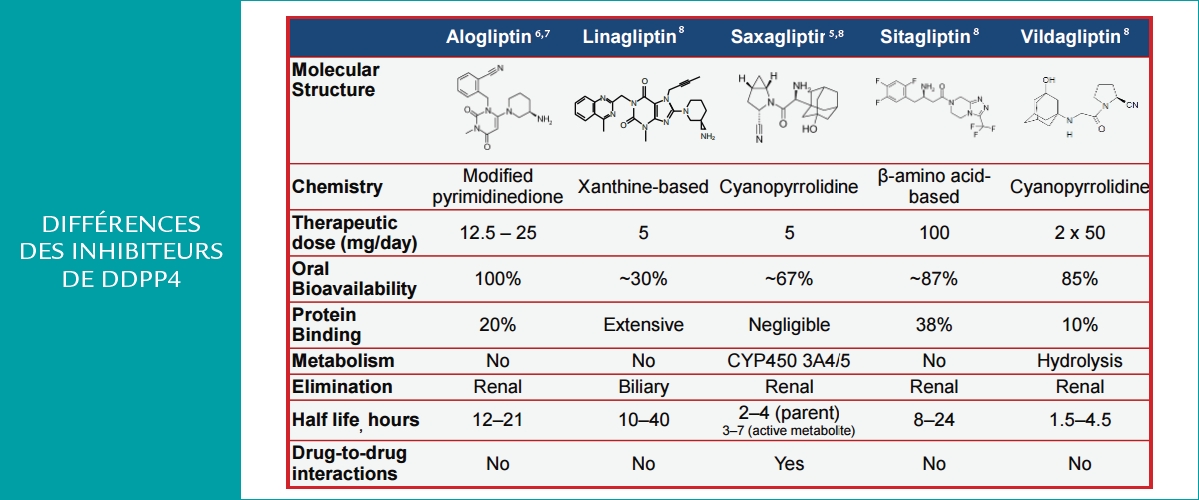
Figure 2
Sécurité cardiovasculaire et inhibiteurs de la DPP4
Les inhibiteurs de la DPP4 ont démontré leur capacité d’abaisser la glycémie et sont reconnus comme n’engendrant pas de prise pondérale et comme déterminant peu d’épisodes d’hypoglycémie. Leur sécurité cardiovasculaire a été explorée dans 2 grandes études de non infériorité versus placebo, conduites avec la saxagliptine et l’alogliptine, SAVOR-TIMI 53(5) et EXAMINE(6), (voir communication de F. Zannad).
D’autres essais de sécurité cardiovasculaire sont en cours, comme TECOS avec la sitagliptine, CAROLINA avec la linagliptine. Mené durant 2 ans chez 16 492 diabétiques de type 2 à risque cardiovasculaire ou avec déjà des antécédents de maladie cardiovasculaire, SAVOR a conclu à la neutralité de la saxagliptine en comparaison du placebo pour le critère d’évaluation primaire composite de l’essai qui associait décès cardiovasculaires, infarctus du myocarde non fatals et AVC ischémiques non fatals. Cependant, un signal faible, mais statistiquement significatif, d’excès d’hospitalisation pour insuffisance cardiaque (critère secondaire) a été relevé sous saxagliptine (3,5% versus 2,8%, risque relatif de 1,27, p = 0,007). Une analyse complémentaire a suggéré que ce risque pourrait être plus élevé chez les patients déjà à risque d’insuffisance cardiaque, lors de l’entrée dans l’étude, ou avec des taux de BNP élevé. Cette augmentation d’hospitalisation pour des insuffisances cardiaques n’a pas été retrouvée dans une analyse post-hoc de l’étude EXAMINE, qui a randomisé 5 380 diabétiques de type 2 avec un syndrome coronaire aigu (SCA) récent (15 à 90 jours précédents la randomisation), l’alogliptine se montrant non inférieure au placebo. Aucun accroissement significatif du nombre de pancréatites aiguës ou chroniques n’a été déploré dans SAVOR ou EXAMINE. La méta-analyse de Shiying Wu(8) et al., qui a pris en compte 50 essais ayant rassemblé 55 141 sujets, a conclu certes à la neutralité des inhibiteurs de DPP4 en termes de mortalité globale et de mortalité cardiovasculaire, de nombre de SCA et d’AVC mais a rapporté une augmentation du nombre d’hospitalisations pour insuffisance cardiaque : risque relatif de 1,16 (1,01-1,33, p = 0,04, n = 39953). Ce qui montre qu’il est nécessaire de suivre le risque d’insuffisance cardiaque.
Analyser la sécurité cardiovasculaire est difficile
Des accroissements du risque cardiovasculaire ont été décrits avec d’autres médicaments antidiabétiques comme les sulfamides, l’insuline, et bien sûr les glitazones (risque d’insuffisance cardiaque notamment). Ces résultats sont néanmoins très délicats à interpréter car ils discordent selon le type d’étude (observationnelle, randomisée, méta-analyse). Même les essais cliniques ne peuvent toujours répondre à cette question de la sécurité d’emploi, car le comparateur peut, lui-même, être à risque. En pratique, il est important pour le clinicien de s’intéresser à 2 paramètres qui peuvent être associés au risque cardiovasculaire : la prise pondérale et les hypoglycémies, lesquelles peuvent être source de troubles du rythme.
D’après la communication de : Atul Pathak, Clinique Pasteur, Toulouse
Atul Pathak
Dimension clinique : Durabilité de l’efficacité des inhibiteurs de la DPP4 en vie réelle
Analysées, il y a déjà deux décennies, les six premières années de l’étude UKPDS(9) révèlent qu’à la différence de ce que l’on observe dans le diabète de type 1, les diabétiques de type 2 nouvellement diagnostiqués ne développent pas d’insulinopénie. Même lorsque l’équilibre glycémique est dégradé, le taux d’insuline n’est pas notablement modifié, sous traitement hygiéno-diététique, comme sous traitement actif, y compris dans le sous-groupe des diabétiques obèses. Pourtant, l’utilisation du marqueur HOMA, qui intègre la relation entre glycémie et insulinémie, a mis en évidence, dans le diabète de type 2, une dégradation progressive de la fonction bêta pancréatique. Tout se passe donc comme si l’aggravation du dysfonctionnement des cellules bêta ne pouvait accroître l’insulinémie, comme il le faudrait pourtant, pour répondre à l’hyperglycémie qui s’installe.
Une dégradation de la fonction incrétine
La fonction incrétine semble également devenir de moins en moins efficace avec le temps. Ce qui contribue probablement à la progression de ce diabète.
A l’appui de cette hypothèse : une étude rétrospective de Franck P. Alford, et al.(10) , ayant comparé sur 10 ans 19 apparentés de diabétiques de type 2 d’une quarantaine d’années à 18 sujets contrôle, d’âge comparable, sans antécédent familial de diabète. Au cours de la période, 9 des 19 apparentés de diabétiques étaient devenus intolérants au glucose, tandis que les 10 autres sujets apparentés étaient restés normotolérants. Or, chez les premiers, la capacité de sécrétion insulinique en réponse à une charge orale en glucose était diminuée, mais le test de réponse insulinique à une charge intraveineuse en glucose ne différait pas de celui des 2 autres groupes. Des résultats que l’on peut interpréter comme liés à une fonction incrétine altérée chez les apparentés de diabétiques de type 2 devenus intolérants au glucose.
Durabilité et IDPP4
L’étude ADOPT a été l’une des premières à aborder le terme de durabilité glycémique après utilisation en monothérapie de la metformine, du glyburide ou de la rosiglitazone(11).
La durabilité était définie par le temps à partir duquel on observait une glycémie dépassant 1,8 g/l, après une nuit de jeune. Ce qui a mis en évidence la supériorité de la rosiglitazone, sur la metformine et le glyburide.
Depuis, le concept de durabilité a évolué et celle-ci est actuellement comprise comme la capacité à assurer un contrôle métabolique au long cours.
La durabilité de l’alogliptine a été comparée, à 2 doses 12,5 mg/j et 25 mg/j, à un sulfamide, le glipizide, dont le dosage a été compris entre 5 et 20 mg /j dans l’étude ENDURE. Cet essai a recruté 2 369 diabétiques de type 2, mal contrôlés sous metformine, aux caractéristiques habituelles (âge moyen de 55,4 ans, HbA1c de 7,6%)(12). Le critère de jugement primaire était la variation d’HbA1c après 1 an et 2 ans de traitement. Cependant, l’étude a également pris en compte le recours à un traitement de sauvetage, qui était instauré dès que le taux d’HbA1c était égal ou dépassait 8,5% entre 20 et 26 semaines, 8% (ou un taux d’HbA1C correspondant à une amélioration de moins de 0,5%) entre 26 et 52 semaines, 7,5% (ou une amélioration de moins de 0,5%) au delà de 1 an. La réduction moyenne du taux d’HbA1c a été respectivement de : – 0,68%, – 0,72% et – 0,59% à 2 ans pour les bras alogliptine 12,5, 25 mg et le glipizide : non infériorité par rapport au glipizide pour les 2 doses d’alogliptine (p < 0,001), supériorité pour la dose de 25 mg/j (p = 0,01) (Figure 3).
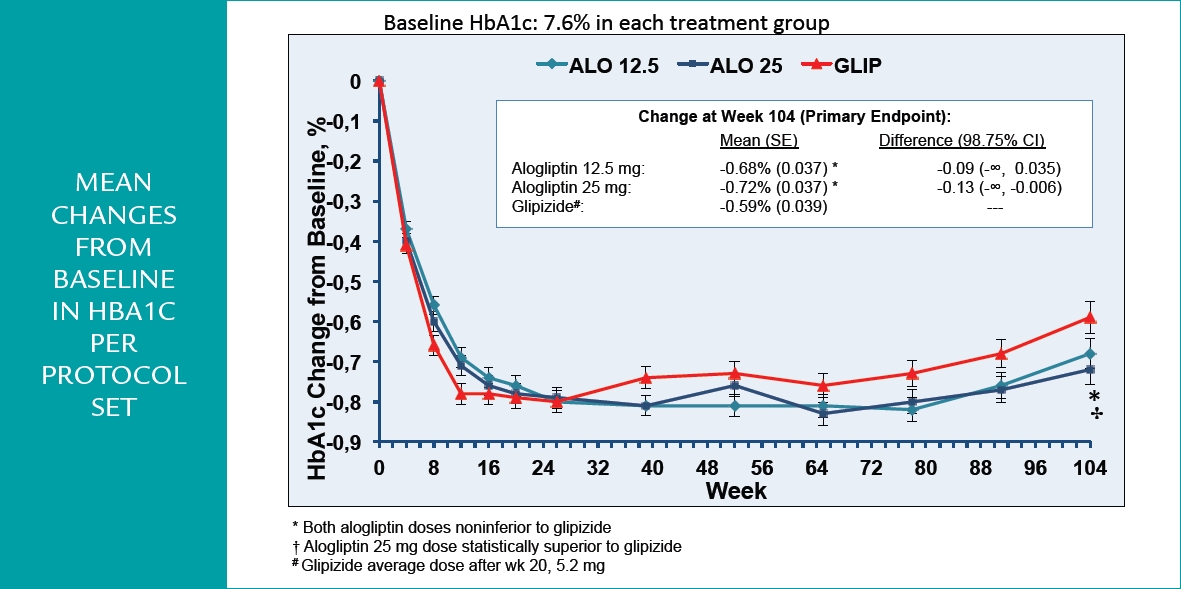
Figure 3
Le pourcentage de patients diabétiques ayant atteint la cible glycémique de moins de 7% de HbA1c était assez proche dans les 3 groupes avec une supériorité pour l’alogliptine 25 mg (48,5% contre 42,8% pour le sulfamide, p = 0,004). Au seuil de 6,5%, les 2 doses d’alogliptine faisaient significativement mieux que le sulfamide (24,1% sous 25 mg, p = 0,004; 23,5% sous 12,5 mg p = 0,019, contre 19% sous glipizide) ; 26,3% des patients du bras 12,5 mg d’alogliptine, 26,9% du bras glipizide, et 22,7% des patients du bras alogliptine 25 mg ont nécessité un traitement de sauvetage.
D’autres études, entreprises avec d’autres médicaments, laissent penser que les inhibiteurs de DPP4 sont au moins équivalents et, peut-être, un peu plus durables que les sulfamides, en termes de seuil d’HbA1c. La question, qui se pose, est de savoir si cette durabilité accrue a une traduction microvasculaire.
D’après la communication de : Samy Hadjadj, CHU de Poitiers
Samy Hadjadj
Dimension cardiovasculaire : Quid des nouvelles thérapies ?
La nécessité de contrôler l’hypertension artérielle et de réduire le taux de LDL-cholestérol pour abaisser la morbi- mortalité cardiovasculaire est largement démontrée. En revanche, il n’est pas certain que le contrôle glycémique ait un tel effet positif chez les diabétiques, même si une relation existe entre taux d’HbA1c et événements micro et macrovasculaires.
Les agences réglementaires, américaine et européenne, ne requièrent qu’une baisse du taux d’HbA1c pour approuver les médicaments antidiabétiques sans exiger de preuves d’efficacité cardiovasculaire, qui apporteraient pourtant des informations essentielles. Cependant, depuis 2008, et les résultats décrits avec la rosiglitazone, des essais de sécurité cardiovasculaire doivent être entrepris pour tout nouvel antidiabétique.
Ces études, dont le nombre dépasse la dizaine, incluent ou vont inclure 115 000 patients. Mais, ont comme critère de jugement principal composite : décès cardiovasculaires, infarctus du myocarde non fatals et AVC non fatals.
Inhibiteurs de DPP4 et insuffisance cardiaque
Deux essais de sécurité cardiovasculaire ont été conduits avec des inhibiteurs de DPP4 : Savor-TIMI 53(5) avec la saxagliptine, EXAMINE(6) avec l’alogliptine.
L’étude Savor a inclus plus de 16000 patients, moins à risque globalement que ceux d’EXAMINE, car pour être inclus ils pouvaient avoir des antécédents de maladie cardiovasculaire ou être seulement considérés comme à risque cardiovasculaire. Ces diabétiques de type 2 ne présentaient pas d’insuffisance cardiaque décompensée mais pouvaient avoir une insuffisance cardiaque compensée. Aucune différence significative n’a été relevée pour le critère de jugement principal. Mais, un excès d’hospitalisations pour insuffisance cardiaque a été constaté précocement dans le bras saxagliptine.
Cet excès d’insuffisance cardiaque n’a pas été retrouvé dans une analyse post-hoc de l’étude EXAMINE(6,7), dont les 5 380 diabétiques inclus avaient été victimes d’un SCA récent et sont donc actuellement la population la plus à risque de tous les essais de sécurité cardiovasculaire réalisés jusqu’ici avec des médicaments antidiabétiques.
Aucun excès de risque relatif n’a, plus particulièrement, été observé pour le critère composite associant hospitalisation pour insuffisance cardiaque et décès cardiovasculaires, qui est plus rigoureux que le simple paramètre hospitalisation car il permet d’éliminer un « biais de survie », en comptabilisant les insuffisants cardiaques décédés (risque relatif de 1,0 ; 0,82-1,21). Cette conclusion n’était pas modifiée, que les patients aient ou non des antécédents d’insuffisance cardiaque, ou que leur taux de BNP se situe dans le quartile le plus élevé.
Il n’a pas non plus été observé, sous alogliptine, de modification notable des taux de NT-proBNP à 6 mois par rapport au placebo, en présence ou non d’antécédents d’insuffisance cardiaque, ni d’augmentation de prescription de diurétique de l’anse, qui témoigne du développement d’une insuffisance cardiaque.
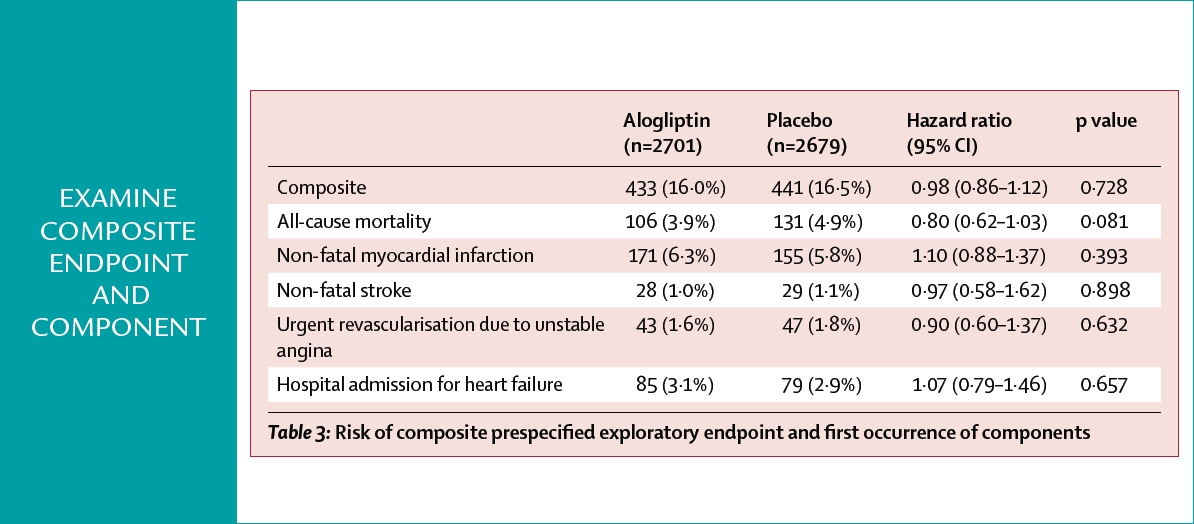
Figure 4
Une relation pas forcément causale
En dépit des données de SAVOR, il n’est cependant pas établi que certains inhibiteurs de DPP4 puissent induire une insuffisance cardiaque et il est possible que le léger accroissement de risque trouvé dans cette étude soit imputable à de simples fluctuations statistiques. Les effets pharmacologiques ne plaident, en effet, pas, en faveur, d’une telle responsabilité des inhibiteurs de DPP4, car cette classe a mis en évidence des effets cardioprotecteurs dans les travaux expérimentaux, le BNP étant lui-même un substrat de la DPP4. Enfin, la DPP4 est un excellent indice pronostique de l’insuffisance cardiaque laquelle est d’autant plus grave que les taux de DPP4 sont élevés. L’étude TECOS, menée avec la sitagliptine, dont les résultats sont attendus pour juin 2015, devrait permettre d’en savoir plus sur cette question importante.
D’après la communication de Faiez Zannad, CHU de Nancy.
Faiez Zannad
RÉFÉRENCES
1. Inzucchi SE, Bergenstal RM, Buse JB, et al. Management of hyperglycemia in type 2 diabetes: a patient-centered approach. Position statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2012;35:1364–79.
2. Inzucchi SE, Bergenstal RM, Buse JB, et al. Management of hyperglycemia in type 2 diabetes, 2015: a patient-centered approach: update to a position statement of the American Diabetes Association and the European Association for the Study of Diabetes. Diabetes Care. 2015;38:140-9.
3. Haute autorité de santé. Patient et professionnels de santé : décider ensemble. Concept, aides destinées aux patients et impact de la « décision médicale partagée ». Octobre 2013.
4. Stacey D, Légaré F, Col NF, et al. Decisions aids for people facing health treatment or screening decisions. Cochrane Database Syst Rev. 2014 Jan 28;1:CD001431.
5. Scirica BM, Bhatt DL, Braunwald E, et al. Saxagliptin and cardiovascular outcomes in patients with type 2 diabetes mellitus. N Engl J Med. 2013;369:1317-26.
6. White WB, Cannon CP, Heller SR, et al. Alogliptin after acute coronary syndrome in patients with type 2 diabetes. N Engl J Med. 2013;369:1327-35.
7. Zannad F, Cannon CP, Cushman WC, et al. Heart failure and mortality outcomes in patients with type 2 diabetes taking alogliptin versus placebo in EXAMINE: a multicentre, randomised, double-blind trial. Lancet. 2015 Mar 9. pii: S0140-6736(14)62225-X.
8. Wu S, Hopper I, Skiba M, Krum H. Dipeptidyl peptidase-4 inhibitors and cardiovascular outcomes: meta-analysis of randomized clinical trials with 55,141 participants. Cardiovasc Ther. 2014;32:147-58.
9. U.K. prospective diabetes study 16. Overview of 6 years’ therapy of type II diabetes: a progressive disease. U.K. Prospective Diabetes Study Group. Diabetes. 1995; 44: 1249-58.
10. Alford FP, Rantzau C, Henriksen JE, et al. Endogenous incretin hormone augmentation of acute insulin secretion in normoglycemic relatives of type 2 diabetic subjects: a 10-year retrospective pathophysiological study. J Clin Endocrinol Metab. 2014.;99:E1943-50.
11. Kahn SE, Haffner SM, Heise MA, et al. Glycemic durability of rosiglitazone, metformin, or glyburide monotherapy. N Engl J Med. 2006;355:2427-43.
12. Del Prato S, Camisasca R, Wilson C, Fleck P. Durability of the efficacy and safety of alogliptin compared with glipizide in type 2 diabetes mellitus: a 2-year study. Diabetes Obes Metab. 2014;16:1239-46.
Article publié dans le supplément du Cordiam N°6 (Mai-Juin 2015)
