
Schématiquement, les anticoagulants oraux directs (AOD) peuvent être utilisés pour la prise en charge de la maladie coronaire soit pour potentialiser le traitement antithrombotique afin de réduire les évènements ischémiques majeurs (au prix d’une légère augmentation des complications hémorragiques) soit comme alternative aux anti-vitamines K (AVK) pour réduire les complications hémorragiques en cas d’association d’antithrombotiques (antiagrégants plaquettaires et anticoagulants).
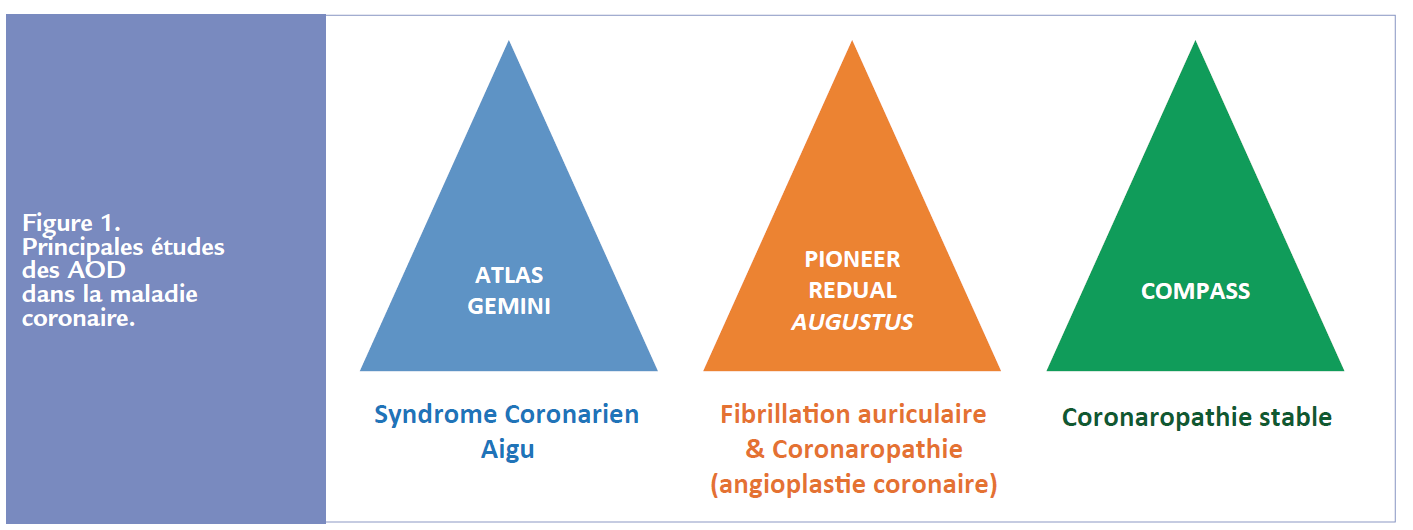
En pratique, il convient de distinguer trois situations :
- lors de la prise en charge initiale des syndromes coronariens aigus (SCA) ;
- en cas d’angioplastie coronaire chez les patients ayant une fibrillation auriculaire (FA) ;
- chez les patients coronariens stables à haut-risque cardiovasculaire (CV) Figure 1.
Pourquoi associer des anticoagulants aux anti agrégants plaquettaires dans la maladie coronaire ?
L’optimisation du traitement antithrombotique chez les patients coronariens pour tenter de réduire la survenue d’évènements ischémiques (ou hémorragiques) peut s’envisager de différentes façons :
◊ En utilisant des anti agrégants plaquettaires plus puissants comme c’est le cas avec les nouveaux inhibiteurs du P2Y12 (Ticagrelor, Prasugrel) qui ont démontré chacun leur supériorité par rapport au traitement de référence (le clopidogrel) sur la survenue des décès CV, des récidives d’infarctus du myocarde (IDM) ou des accidents vasculaires cérébraux (AVC) au décours d’un SCA .
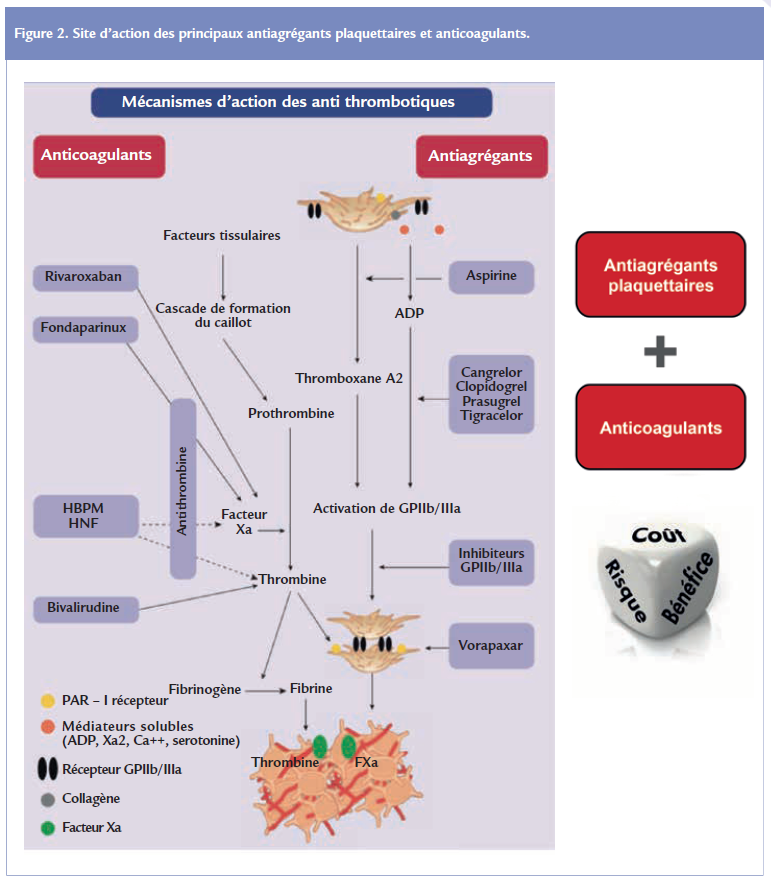
◊ En associant aux anti agrégants plaquettaires, un traitement synergique (les anticoagulants). Dans ce cas, les AODs semblent plus intéressants que les AVK car ils inhibent de façon spécifi que les facteurs de la coagulation activés qui sont soit la thrombine (facteur IIa ; avec le dabigatran), soit le facteur de Stuart activé (facteur Xa ; avec le rivaroxaban et l’apixaban) engendrant moins de complications hémorragiques Figure 2.
En cas de nécessité d’un traitement par anticoagulant (FA …) les AODs semblent donc être une bonne option. L’arrivée prochaine des antidotes (puisqu’actuellement seul le dabigatran en a un disponible sur le marché) devrait libéraliser leur prescription dans cette indication.
Les bénéfices cliniques sont bien entendu à pondérer en fonction des complications hémorragiques (inéluctables) et des surcôuts engendrés par l’association de ces traitements.
Existe-il vraiment une place pour les AOD dans la prise en charge initiale des syndromes coronariens aigus ?
ATLAS-ACS 2TIMI 51 est l’étude pivot ayant validé l’intérêt des AOD à faibles doses dans la prise en charge des SCA stabilisés (entre le 1er et 14ème jour) et à faible risque hémorragique (1).
Dans cette étude, l’ajout d’une petite dose de rivaroxaban (2.5mg deux fois par jour) associée à la double anti agrégation plaquettaire classique (aspirine et clopidogrel) a permis de réduire la survenue d’évènements cardiovasculaires (décès CV, IDM, AVC) de 26% (HR 0.84 ; 95% IC 0.74-0.96) sans augmentation significative des complications hémorragiques majeures.
Pourtant, malgré des résultats probants (bénéfi ces observés également sur la mortalité CV et globale) cette stratégie ne s’est pas développée.
Ceci peut s’expliquer par les résultats concomitants des études PLATO et TRITON qui ont respectivement démontré la supériorité du ticagrelor et du prasugrel par rapport au clopidogrel remettant ainsi en question la double anti agrégation plaquettaire habituelle (2, 3). La stratégie proposée par ATLAS-ACS 2 TIMI 51 reste toutefois une option thérapeutique envisageable (niveau de preuve : IIB-B dans les dernières recommandations).
Plus récemment, l’étude GEMINI-ACS 1 (étude de sécurité de phase II), a démontré que le ticagrelor (qui est devenu aujourd’hui l’anti agrégant plaquettaire le plus prescrit en association à l’aspirine dans le SCA) pouvait être utilisé de la même manière que dans l’étude précédente (association de ticagrelor et de rivaroxaban 2.5 mg deux fois par jour) 4.
Même si l’association rivaroxaban à petite dose / inhibiteur du P2Y12 n’est pas dans cette étude inférieure en termes d’évènements hémorragiques majeurs à la stratégie de référence (aspirine / inhibiteur du P2Y12), cette étude n’a pas fait évoluer les pratiques.
En résumé, malgré des résultats intéressants, les AODs ne sont pas aujourd’hui utilisés en pratique courante dans la prise en charge initiale des SCA.
Quels traitements antithrombotiques choisir en cas d’angioplastie coronaire chez un patient ayant une fibrillation auriculaire ?
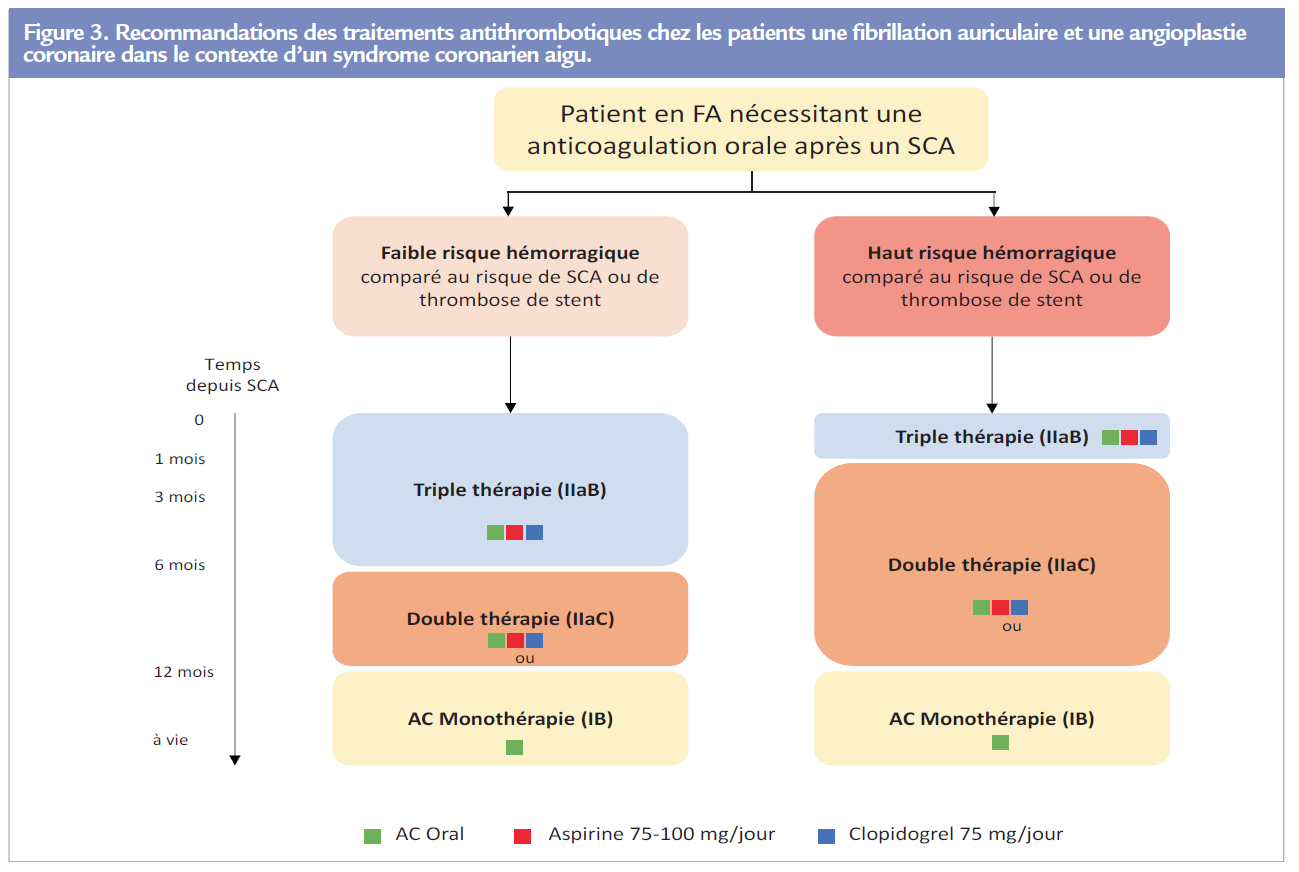
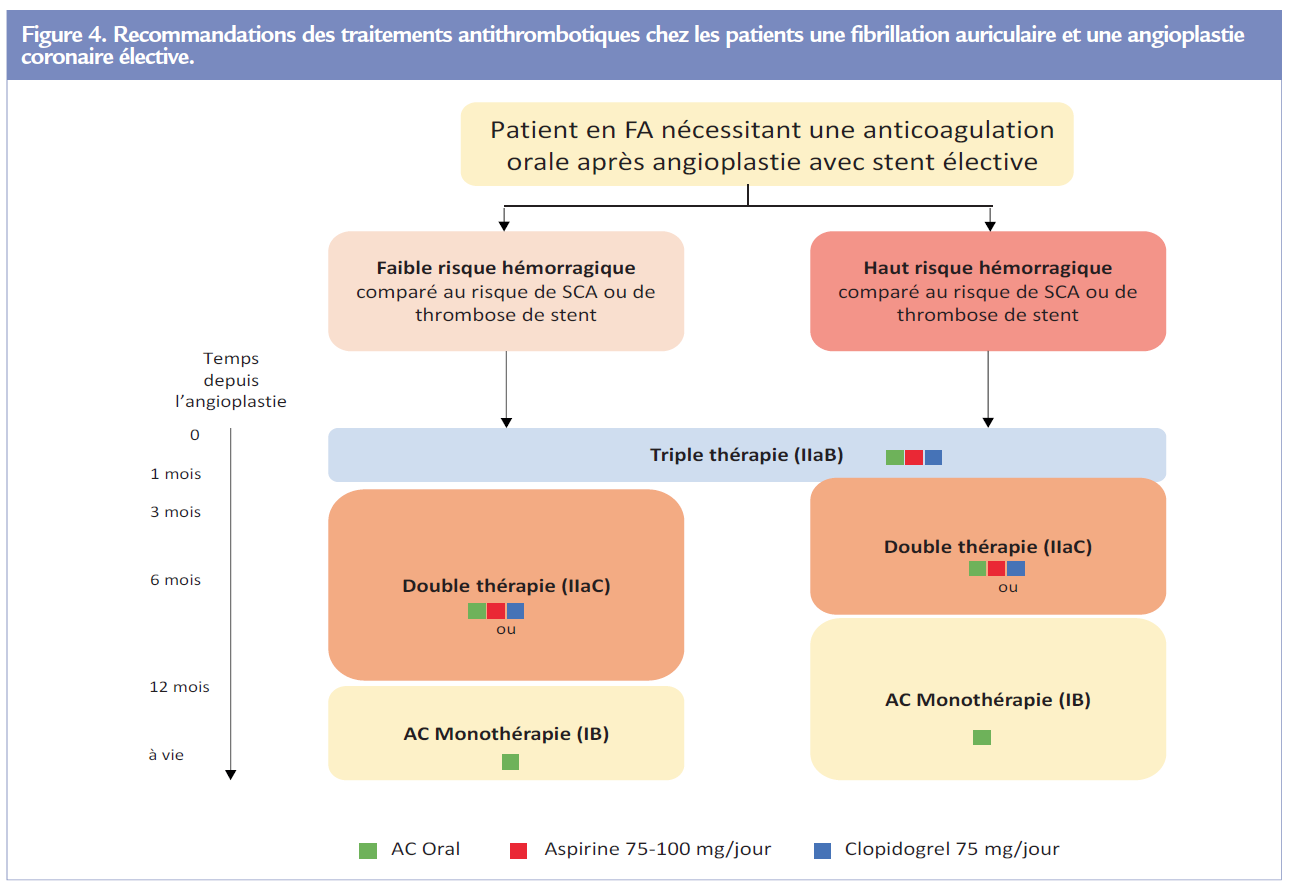
La présence d’une coronaropathie est rapportée dans 20 à 40% des patients ayant une FA. Parmi ces patients, 20 à 40% d’entre eux vont avoir au cours de leur suivi une revascularisation coronaire percutanée. Les recommandations actuelles préconisent l’utilisation d’un anticoagulant (pouvant être un AOD) et varient selon la situation clinique : après un syndrome coronaire aigu Figure 3 ; ou après une angioplastie élective Figure 4 (5). La tendance actuelle est de privilégier un AOD (par rapport aux AVK) et d’interrompre assez précocement l’aspirine aux dépens des autres antithrombotiques. Trois études (PIONEER AF-PCI avec le rivaroxaban, REDUAL PCI avec le DABIGATRAN, et AUGUSTUS avec l’apixaban) apportent des renseignements complémentaires qui vont probablement modifier nos pratiques.
PIONEER AF-PCI, présentée à l’AHA 2016,
Cette étude a évalué chez 2,124 patients ayant une FA, trois stratégies antithrombotiques au décours d’une angioplastie coronaire (dont 40% réalisées en urgence) (6):
◊ association rivaroxaban 15mg – clopidogrel pendant 12 mois ;
◊ association aspirine-clopidogrel (ou ticagrelor) et rivaroxaban 2.5mg (2 fois par jour) pendant 1 à 6 mois puis rivaroxaban 15mg – aspirine jusqu’à 12 mois ;
◊ association antivitamine K- aspirine-clopidogrel (ou ticagrelor) pendant 1 à 6 mois puis AVKaspirine jusqu’à 12 mois.
Les résultats de cette étude montrent une réduction des saignements majeurs (critère principal de l’étude) avec une réduction du risque relatif de l’ordre de 40% avec l’utilisation d’une deux stratégies utilisant le rivaroxaban par rapport au traitement de référence. Pas de différence observée entre les différentes stratégies sur la survenue d’évènements ischémiques majeurs même si l’étude n’était pas prévue pour répondre à cette question.
RE-DUAL-PCI, présentée à l’ESC 2017
Cette étude a évalué chez 2,500 patients ayant une FA, trois stratégies antithrombotiques, initiées au plus tard dans les 72 heures après une angioplastie coronaire (dont environ 40% également réalisées en urgence) 7 :
◊ association dabigatran 150 mg (2 fois par jour), clopidogrel (ou ticagrelor) ;
◊ association dabigatran 110 mg (2 fois par jour), clopidogrel (ou ticagrelor) ;
◊ association aspirine, clopidogrel (ou ticagrelor) et warfarine. Le traitement devait être d’une durée minimale de 6 mois. A noter, l’arrêt de l’aspirine précoce (au décours de l’angioplastie) dans les deux stratégies utilisant le dabigatran.
Les résultats montrent une réduction des saignements majeurs avec l’utilisation du dabigatran (et notamment avec la dose 110 mg avec une réduction du risque relatif de 48%) par rapport au traitement de référence. Enfin, les deux stratégies utilisant du dabigatran étaient non-inférieures au traitement de référence concernant la survenue d’évènements ischémiques (décès, évènements thromboemboliques, ou revascularisation en urgence) bien que l’étude n’était là encore pas conçue pour pouvoir répondre à cette question.
AUGUSTUS
Cette étude actuellement en cours évalue chez 4,600 patients ayant une FA, quatre stratégies antithrombotiques (pour une durée de 6 mois minimum) débutée dans les 14 jours suivant une angioplastie coronaire réalisée en urgence ou de manière programmée:
- association apixaban (2.5 ou 5mg 2 fois par jour) et un inhibiteur du P2Y12 ;
- association apixaban (2.5 ou 5mg 2 fois par jour), un inhibiteur du P2Y12 et l’aspirine ;
- association warfarine et un inhibiteur du P2Y12 ;
- association warfarine, un inhibiteur du P2Y12 et l’aspirine (NCT NCT02415400).
En résumé, ces études mettent les AOD en première ligne chez les patients ayant une FA et devant subir une angioplastie coronaire (urgente ou non) essentiellement en réduisant les complications hémorragiques (sans apporter de signal d’alarme sur la survenue d’évènements ischémiques).
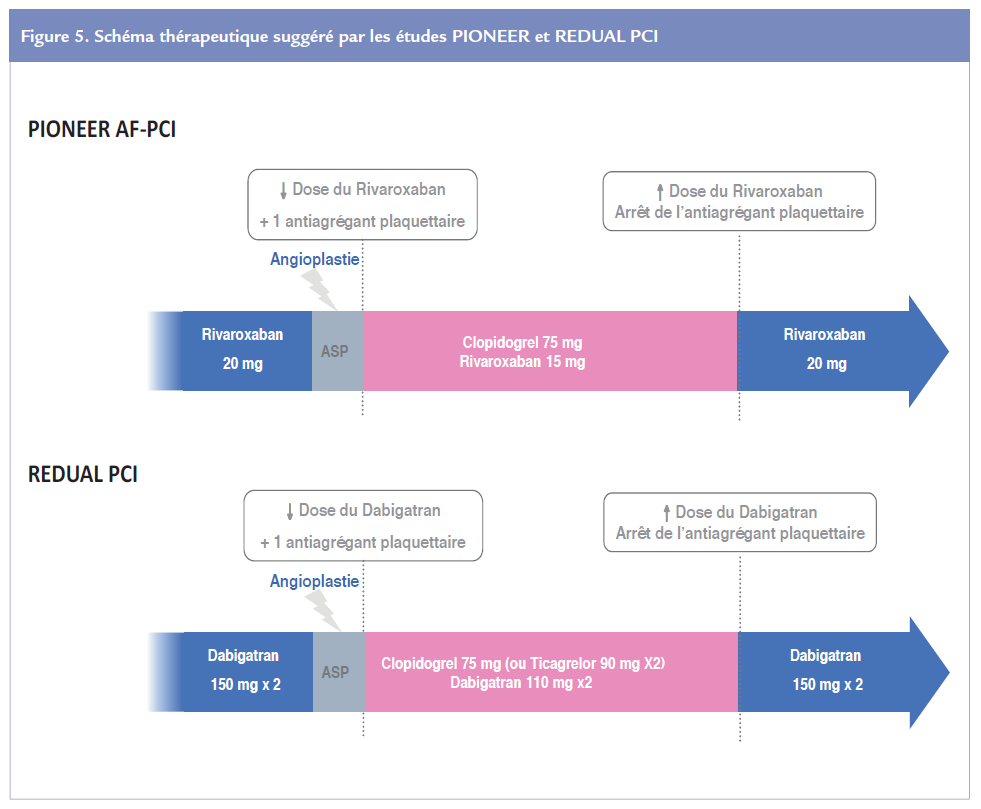
Les deux premières études proposent une alternative aux schémas thérapeutiques actuellement recommandés en privilégiant les AOD et avec un abandon précoce de l’aspirine Figure 5.
L’aspirine restera-il le traitement de fond des coronariens stables ?
L’étude COMPASS, présentée à l’ESC cette année, va probablement remettre en question nos pratiques chez certains patients coronariens « stables » (8). Dans cette étude, près de 30,000 patients ayant un artériopathie périphérique et/ou une coronaropathie à haut risque (définie par un âge ≥65 ans ou un âge inférieur avec des critères d’enrichissement) ont été randomisés en 3 bras :
- aspirine seule (traitement de référence) ;
- rivaroxaban 5mg (2 fois par jour) seul ;
- association aspirine et rivaroxaban 2.5mg (2 fois par jour).
L’étude a été interrompue au cours du recrutement par le comité de surveillance en raison d’une supériorité nette du critère principal (décès CV, IDM, AVC) chez les patients traités par l’association aspirine rivaroxaban à petite dose. A noter également un bénéfice de cette association (par rapport au traitement de référence) sur la mortalité CV (ayant motivé l’interruption de l’étude), les AVC, et les IDM. Ces bénéfices étaient toutefois associés à une augmentation des saignements majeurs de 70% (HR 1.70 (95% : 1.40-2.05) sans occasionner de décès. Il est bien entendu inimaginable de changer le traitement antithrombotique de tous les patients ayant un athérome documenté. Néanmoins, les analyses de sous-groupes permettront très certainement de déterminer les patients les plus « à risque » justifiant cette nouvelle stratégie thérapeutique.
En conclusion, les dernières données de la littérature mettent en avant les AOD chez les patients coronariens notamment en cas de SCA, d’angioplastie coronaire (en cas de FA concomitante) et plus largement tous les coronariens stables ayant un profil de risque élevé.
Etienne Puymirat, Hôpital Européen Georges Pompidou, Paris
Liens d’intérêts (expertises, présentations et/ou bourses) : Amgen, Astra-Zeneca, Bayer, BMS, Biotronik, Daiichi-Sankyo, Lilly, MSD, Pfizer, The Medicine Company, Sanofi , SJM et Servier
RÉFÉRENCES
1. Mega JL, Braunwald E, Wiviott SD, Bassand JP, Bhatt DL, Bode C, Burton P, Cohen M, Cook-Bruns N, Fox KA, Goto S, Murphy SA, Plotnikov AN, Schneider D, Sun X, Verheugt FW, Gibson CM; ATLAS ACS 2–TIMI 51 Investigators. Rivaroxaban in patients with a recent acute coronary syndrome. N Engl J Med. 2012 Jan 5;366(1):9-19.
2. Wallentin L, Becker RC, Budaj A, Cannon CP, Emanuelsson H, Held C, Horrow J, Husted S, James S, Katus H, Mahaffey KW, Scirica BM, Skene A, Steg PG, Storey RF, Harrington RA; PLATO Investigators, Freij A, Thorsén M. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med. 2009 Sep 10;361(11):1045-57.
3. Wiviott SD1, Braunwald E, McCabe CH, Montalescot G, Ruzyllo W, Gottlieb S, Neumann FJ, Ardissino D, De Servi S, Murphy SA, Riesmeyer J, Weerakkody G, Gibson CM, Antman EM; TRITON-TIMI 38 Investigators. Prasugrel versus clopidogrel in patients with acute coronary syndromes. N Engl J Med. 2007 Nov 15;357(20):2001-15.
4. Ohman EM, Roe MT, Steg PG, James SK, Povsic TJ, White J, Rockhold F, Plotnikov A, Mundl H, Strony J, Sun X, Husted S, Tendera M, Montalescot G, Bahit MC, Ardissino D, Bueno H, Claeys MJ, Nicolau JC, Cornel JH, Goto S, Kiss RG, Güray Ü, Park DW, Bode C, Welsh RC, Gibson CM. Clinically signifi cant bleeding with low-dose rivaroxaban versus aspirin, in addition to P2Y12 inhibition, in acute coronary syndromes (GEMINI-ACS-1): a double-blind, multicentre, randomised trial. Lancet. 2017 May 6;389(10081):1799-1808.
5. Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, Castella M, Diener HC, Heidbuchel H, Hendriks J, Hindricks G, Manolis AS, Oldgren J, Popescu BA, Schotten U, Van Putte B, Vardas P, Agewall S, Camm J, Baron Esquivias G, Budts W, Carerj S, Casselman F, Coca A, De Caterina R, Deftereos S, Dobrev D, Ferro JM, Filippatos G, Fitzsimons D, Gorenek B, Guenoun M, Hohnloser SH, Kolh P, Lip GY, Manolis A, McMurray J, Ponikowski P, Rosenhek R, Ruschitzka F, Savelieva I, Sharma S, Suwalski P, Tamargo JL, Taylor CJ, Van Gelder IC, Voors AA, Windecker S, Zamorano JL, Zeppenfeld K. 2016 ESC Guidelines for the management of atrial fi brillation developed in collaboration with EACTS. Eur Heart J. 2016 Oct 7;37(38):2893-2962.
6. Gibson CM, Mehran R, Bode C, Halperin J, Verheugt FW, Wildgoose P, Birmingham M, Ianus J, Burton P, van Eickels M, Korjian S, Daaboul Y, Lip GY, Cohen M, Husted S, Peterson ED, Fox KA. Prevention of Bleeding in Patients with Atrial Fibrillation Undergoing PCI. N Engl J Med. 2016 Dec 22;375(25):2423-2434.
7. Cannon CP, Bhatt DL, Oldgren J, Lip GYH, Ellis SG, Kimura T, Maeng M, Merkely B, Zeymer U, Gropper S, Nordaby M, Kleine E, Harper R, Manassie J, Januzzi JL, Ten Berg JM, Steg PG, Hohnloser SH; RE-DUAL PCI Steering Committee and Investigators. Dual Antithrombotic Therapy with Dabigatran after PCI in Atrial Fibrillation. N Engl J Med. 2017 Oct 19;377(16):1513-1524
8. Eikelboom JW, Connolly SJ, Bosch J, Dagenais GR, Hart RG, Shestakovska O, Diaz R, Alings M, Lonn EM, Anand SS, Widimsky P, Hori M, Avezum A, Piegas LS, Branch KRH, Probstfi eld J, Bhatt DL, Zhu J, Liang Y, Maggioni AP, Lopez-Jaramillo P, O’Donnell M, Kakkar AK, Fox KAA, Parkhomenko AN, Ertl G, Störk S, Keltai M, Ryden L, Pogosova N, Dans AL, Lanas F, Commerford PJ, Torp-Pedersen C, Guzik TJ, Verhamme PB, Vinereanu D, Kim JH, Tonkin AM, Lewis BS, Felix C, Yusoff K, Steg PG, Metsarinne KP, Cook Bruns N, Misselwitz F, Chen E, Leong D, Yusuf S; COMPASS Investigators. Rivaroxaban with or without Aspirin in Stable Cardiovascular Disease. N Engl J Med. 2017 Oct 5;377(14):1319-1330.
