La découverte de l’insuline en 1921 a révolutionné le pronostic du patient diabétique de type 1 (Dt1).
Depuis, l’évolution de ce traitement a été majeure : initialement produite par extraction à partir de pancréas de bœuf ou de porc puis synthétisée, l’insuline a connu une avancée avec l’apparition dans les années 2000 des analogues d’insuline permettant d’améliorer leur rapidité d’action. Une étude pédiatrique sur plus de 4 300 enfants participant aux colonies de vacances de l’Association des Jeunes diabétiques a mis en évidence que depuis 1997, l’utilisation des insulines mixtes et des schémas à 3 injections diminuent fortement au profit d’un schéma basal bolus (analogues lent et rapide) ou de la mise sous pompe, permettant de diminuer de moitié le nombre d’enfant ayant une HbA1C supérieure à 9%. En 2011, 18% des enfants et 32% des adultes Dt1 étaient traités par pompe à insuline en France, et en 2014, 45% des enfants participants à ces colonies de vacances étaient sous pompe (1, 2).
Depuis quelques années, le traitement par pompe s’est amélioré avec la mise sur le marché de capteurs. Ceux-ci permettent une mesure en continue de la glycémie interstitielle qui s’affiche sur l’écran de la pompe, ainsi que les tendances glycémiques du patient permettant d’anticiper une hypoglycémie ou une hyperglycémie. A l’heure actuelle, ces capteurs ne sont pas remboursés et sont donnés au cas par cas en discontinu lors d’évènements particuliers (marathon, grossesse, hypoglycémies non ressenties ou déséquilibre non expliqué, par exemple). Petit à petit, on tend vers l’administration de l’insuline en boucle fermée, tel un pancréas artificiel. Aujourd’hui, certaines associations pompe-capteur proposent un arrêt de la pompe en cas de glycémie passant en dessous d’un seuil prédéfini. Puis progressivement, sont publiés des essais de boucle
fermée. Différents algorithmes permettent de programmer le débit basal de la pompe en fonction de la glycémie mesurée par ce capteur. Ceci conduirait à un pancréas artificiel avec une administration d’insuline en circuit fermé adapté à la glycémie du patient (Figure 1).
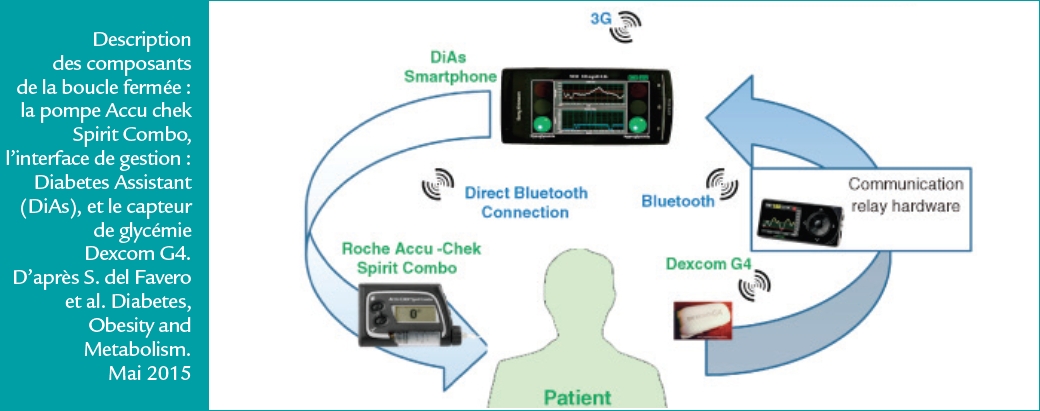
Figure 1
Si son utilisation a montré son efficacité la nuit, le système n’est pas capable d’anticiper et de gérer les grandes variations de glycémie au moment des repas, ce qui nécessite donc d’administrer manuellement les bolus au moment des repas. Deux études ont été présentées démontrant que l’utilisation de circuit fermé la nuit améliore la glycémie principalement en fin nuit, avec une diminution du nombre d’hypoglycémie, une réduction de moitié du temps passé en hypoglycémie. Même si le temps passé dans l’intervalle-cible de normoglycémie augmente de 10% seulement, le bénéfice de la boucle fermée nocturne améliore également le profil glycémique le jour (3, 4). Dans la littérature, d’autres équipes ont évalué l’intérêt de cette boucle fermée jour et nuit avec administration manuelle des bolus pour les repas, ce qui permet d’obtenir une amélioration plus marquée des mêmes paramètres (5).
Si on est encore un peu loin du pancréas artificiel, un autre traitement en cours de développement est la greffe d’ilot. Cette greffe n’est actuellement proposée que dans le cadre de protocole, et réservée à des patients ayant un diabète très instable, faisant des hypoglycémies non ressenties fréquentes et invalidantes ou à des patients diabétiques ayant bénéficié d’une greffe de rein. Ce traitement nécessite 2 à 3 donneurs en état de mort encéphalique pour une infusion d’ilots.
Les ilots sont purifiés, isolés, injectés dans la veine porte, et vont s’emboliser dans la microcirculation hépatique. Actuellement 700 patients ont bénéficié de ce traitement en France. Il existe un réseau « GRAGIL », regroupant plusieurs centres (Grenoble, Lyon, Besançon, Genève, Nantes, Strasbourg, Montpellier, Nancy, et Clermont-Ferrand), qui se place au 3ème rang mondial des greffes d’ilots. Cependant, ce traitement ne « guérit » pas le patient de son diabète puisqu’il ne permet l’obtention d’une insulino-indépendance que chez 52% des patients avec une durée médiane d’insulinoindépendance de 18 mois. Quoiqu’il en soit, l’effet est majeur sur les hypoglycémies sévères : pour des patients faisant en moyenne avant la greffe 5 épisodes d’hypoglycémie sévère dans l’année, 90% ne décrivent plus d’hypoglycémie sévère et cet effet perdure dans le temps. Si l’insulino-indépendance n’est pas toujours atteinte, l’équilibre glycémique est très nettement amélioré puisque 2/3 des patients normalisent leur HbA1C à 1 an et cet effet est maintenu à 5 ans. Les complications de ce traitement sont élevées : 32% des patients décrivent des effets indésirables liés à l’immunosuppression et 12% liés aux complications du geste (thrombose portale, hémopéritoine). 67% des effets indésirables sont considérés comme graves et 9% menaçant le pronostic vital. Si ce traitement est efficace pour améliorer l’équilibre glycémique, il reste réservé à certains patients ayant un diabète instable. Les protocoles d’immunosuppression et les techniques d’infusion d’ilots sont encore à améliorer avant d’élargir les indications de ce traitement.
Modérateurs : P-Y. Benhamou (Grenoble) et P. Barat (Bordeaux)
Claire Briet
RÉFÉRENCES
1. Sulmont V, Lassmann-Vague V, Guerci B, Hanaire H, Leblanc H, Leutenegger E, Mihaileanu M, Tubiana-Rufi N; French pediatric PUMP group. Access of children and adolescents with type 1 diabetes to insulin pump therapy has greatly increased in France since 2001. Diabetes Metab. 2011 Feb;37(1):59-63.
2. SFD 2015. Communication orale 08 : J.-J Robert, M. Keller, R. Attia, J. Djadi-Prat, M. Cahané, C. Choleau. HbA1C, schéma thérapeutiques, connaissances et qualité de vie chez les enfants et les adolescents ayant un diabète de type 1
3. SFD 2015. Communication orale 10 : A. Paillard. P. Maxime, M. Penet, M-A. Lefebvre, M. Carpentier, A. Esvant, A-M. Leguerrier, I. Guilhem, J.-Y. Poirier. Une nouvelle loi de commande vers le pancréas artificiel : SP-MPC (Saddle Point Model Predictive Control), première étude clinique
4. SFD 2015. Communication orale 11 : E. Renard, J. Place, O. Diouri, A. Farret, Consortium Ap At home (Montpellier). Insulinothérapie en boucle fermée à domicile en période vespérale et nocturne durant 2 mois, données préliminaires française de l’essai randomisé contrôlé HYBRID.
5. Leelarathna L, Dellweg S, Mader JK, Allen JM, Benesch C, Doll W, Ellmerer M, Hartnell S, Heinemann L, Kojzar H, Michalewski L, Nodale M, Thabit H, Wilinska ME, Pieber TR, Arnolds S, Evans ML, Hovorka R; AP@home Consortium. Day and night home closed-loop insulin delivery in adults with type 1 diabetes: three-center randomized crossover study. Diabetes Care. 2014 Jul;37(7):1931-7.
Article publié dans le supplément du Cordiam N°6 (Mai-Juin 2015)
