Pathologie infectieuse virale apparue à la fi n de l’année 2019 en Chine, la COVID-19 a été diagnostiquée initialement à partir de ses formes respiratoires. Ses manifestations cliniques sont en fait très variées , notamment du fait de son polymorphisme physiopathologique qui peut toucher différents organes, dont le cœur. Initialement ténues les relations entre infection à SARS-CoV-2 et rythmologie se sont progressivement précisées, et semblent concerner surtout les formes sévère et les effets arythmogènes de certains médicaments proposés pour son traitement . Par ailleurs cette pandémie, du fait des contraintes qu’elle a imposées dans l’organisation des soins au pic de la crise sanitaire a modifié les modalités de prise en charge rythmologique des patients et a induit vraisemblablement, notamment lors du confinement , un retard diagnostique et thérapeutique des arythmies. Elle a aussi permis de faire évoluer nos pratiques, et ce de façon certainement pérenne, vers le développement des systèmes connectés et vers un raccourcissement des durées d’hospitalisation pour les procédures interventionnelles.
Epidémiologie et nature des arythmies lors de l’infection à SARS-CoV-2
S’il n’existe pas d’arythmie ni de modification électrocardiographique spécifiques de la COVID-19, il n’en reste pas moins que différents types de troubles du rythme et d’anomalies ECG ont été rapportés soit à l’admission des patients hospitalisés, mais il est alors parfois difficile de faire la part de ce qui est imputable à la COVID-19 ou à une cardiopathie préexistante méconnue, soit au cours de l’évolution de l’infection par le SARS-CoV-2.
Des palpitations sont présentes chez 10% des patients hospitalisés, pouvant parfois même révéler la maladie, ainsi que des lipothymies/syncopes. Dans une enquête internationale réalisée auprès d’électrophysiologistes et qui a inclu 915 patients hospitalisés pour la COVID-19, les arythmies supraventriculaires étaient plus fréquemment observées (26% des patients) que les ventriculaires (16 % des patients) mais sans qu’il soit précisé si ces arythmies préexistaient ou étaient apparues de novo. Or une majorité des patients sévères infectés par le SARS-CoV-2 sont âgés et souvent porteurs de comorbidités qui peuvent être une source d’arythmies méconnues. Ainsi un antécédent de fibrillation atriale (FA) est présent chez 1 à 7 % des patients hospitalisés. Dans une série rétrospective incluant 138 patients COVID-19 hospitalisés à Wuhan, Wang et al ont rapporté la survenue d’arythmies dans 16,7% des cas, avec une incidence significativement plus élevée chez les patients amenés à séjourner en réanimation (44,4%) que chez ceux restés en hospitalisation conventionnelle (6,9 %, p<0,01), néanmoins la nature et la durée de ces arythmies ne sont pas détaillées. Dans une série américaine plus récente incluant 700 patients COVID-19 hospitalisés et télémétrés l’incidence des arythmies, qui sont donc bien documentées, est néanmoins plus faible (7,6%) .
L’incidence de survenue d’une FA de novo chez les patients hospitalisés varie de 3,6 % à 8 % . Elle est plus élevée chez les patients en réanimation , notamment ceux requérant une ventilation mécanique que chez ceux n’en ayant pas besoin (17,7% versus 1,9%). En fait l’intérêt des cliniciens s’est concentré sur les arythmies ventriculaires du fait de leur risque vital potentiel. Dans une série rétrospective de 191 patients COVID-19 hospitalisés à Wuhan, Guo et al ont rapporté une incidence de 6 % d’arythmies ventriculaires sévères (TV/FV). Ces arythmies surviennent plus fréquemment chez les patients ayant une élévation de la troponine au delà du 99ème percentile (17,3%) que chez ceux qui n’en ont pas (1,5%, p<0.001). La physiopathologie de ces TV/FV est souvent multifactorielle, pouvant résulter d’une atteinte myocardique directe ou secondaire à l’orage cytokinique ou à une ischémie, à laquelle peuvent s’ajouter une stimulation catécholergique intense, des perturbations métaboliques, respiratoires et hémodynamiques en cas de défaillance multi-organes plutôt que d’une atteinte directe du SARS-CoV-2. A ces facteurs aigus liés à l’infection par le SARS-CoV-2 peuvent s’ajouter la présence d’une cardiopathie structurelle ou rythmique, qui préexiste chez 8 à 18 % de ces sujets souvent âgés et les effets arythmogènes des médicaments administrés. Néanmoins l’incidence des ces arythmies ventriculaires sévères semblent être moins importante que ce qui avait été initialement rapporté dans les séries chinoises. Dans leur série de 700 patients télémétrés Bhatla et al n’ont observés que des TV non-soutenues (1,4%) et un cas de torsade de pointe sans autre arythmie ventriculaire soutenue.
Par ailleurs les arythmies ventriculaires sévères ne représentent que 5,9 à 11 % des causes d’arrêt cardio-circulatoire (ACR) intra-hospitaliers qui ont été pris en charge précocement (<1 min), la majorité de ces ACR résultant en fait d’une dissociation électromécanique ou d’une asystolie. Des bradycardies sinusales et des troubles conductifs auriculo-ventriculaire (AV) de degrés variables ont été observés chez 7 % des patients COVID-19 hospitalisés, mais sans que leur chronologie de survenue soit précisée. Ils semblent en fait peu fréquents au cours de l’évolution et les quelques cas de BAV complet rapportés sont souvent transitoires , survenant chez des patients intubés ventilés. Ainsi bien que à 87,9 % des ACR intra-hospitaliers soient dus à des asystolies, celles-ci surviennent dans la majorité des cas comme la conséquences de la détresse respiratoire et non comme une conséquence rythmique directe de l’infection par SARS-CoV-2.
Quelques publications se sont intéressées aux modifications de l’ECG observées chez les patients COVID-19 hospitalisés soit à leur admission, soit lors de l’évolution. Chez 112 patients infectés par le SARs-CoV-2 Deng et al rapportent la présence d’une tachycardie sinusale dans 30 % des cas, le plus souvent dans les formes cliniquement sévères. Néanmoins l’amplitude de cette tachycardie est moindre que celle attendue pour le niveau de fièvre observée, comme cela a déjà été décrit dans d’autres infections virales.
Les modifications ECG les plus habituelles consistent en des anomalies non spécifiques de la repolarisation qui apparaissent chez 14 à 19 % des patients souvent à distance du début des symptômes. Elles sont essentiellement observées en phase d’élévation des biomarqueurs cardiaques (Troponine et BNP) , et résultent d’une atteinte myocardique directe ou secondaire (hypoxie, ischémie, inflammatoire…) ou d’une atteinte péricardique. Parfois très marquées elles peuvent mimer un SCA ST+ sans que ne soit retrouvées de lésions coronaires significatives. L’ECG initial objective des anomalies (hypertrophie, modification du ST-T, …) chez 30 % des patients qui peuvent être des stigmates de cardiopathies structurelles ou électriques méconnues comme un syndrome de Brugada démasqué par la fièvre ou un syndrome du QT long qui peuvent majorer le risque rythmique de la COVID-19 et en modifier la prise en charge thérapeutique.
Traitement des arythmie chez les patients COVID-19
Les stratégies thérapeutiques anti-arythmiques chez les patients COVID-19 sont très proches de celles appliquées à la population générale et sont bien détaillées dans le guide de l’ESC sur les conséquences cardio-vasculaires de l’infection à SARS-CoV-2. Néanmoins de par les particularités de cette pandémie, elles s’en écartent par quelques points. Le contexte de crise sanitaire au pic de la pandémie a modifié les indications de rythmologie interventionnelle, d’une part en restreignant la disponibilité en matériel, en salles de cathétérisme et en personnel soignant dédié (notamment en anesthésie-réanimation), d’autre part en incitant à réduire le risque de contamination des soignants et des patients. Ceci a conduit à établir une classification du degré d’urgence de chaque procédure rythmologique interventionnelle (Tableau 1) afin de ne réaliser que celles identifiées comme réellement urgentes et de différer les autres à une période où la crise sanitaire sera résolue. Les prises en charge thérapeutiques non-ablatives ont été ainsi privilégiées, notamment pour les arythmies supra-ventriculaires sans risque vital immédiat. Par ailleurs des options pharmacologiques un peu différentes de celles habituellement utilisées ont été proposées chez les patients en réanimation avec atteinte multiorganes en raison de la fréquence des récidives précoces des arythmies et des interactions pharmacologiques avec certains des médicaments utilisés contre le SARSCoV-2. Néanmoins les recommandations soulignent l’importance de réévaluer les stratégies thérapeutiques, notamment en termes d’ablation, une fois que les conditions sanitaires permettent de récupérer les capacités interventionnelles Ainsi la prise en charge des arythmies atriales et ventriculaire survenant lors de l’infection par le SARS-CoV-2 a fait l’objet d’algorithmes basés sur la tolérance hémodynamique de l’arythmie et les traitements de la COVID-19.
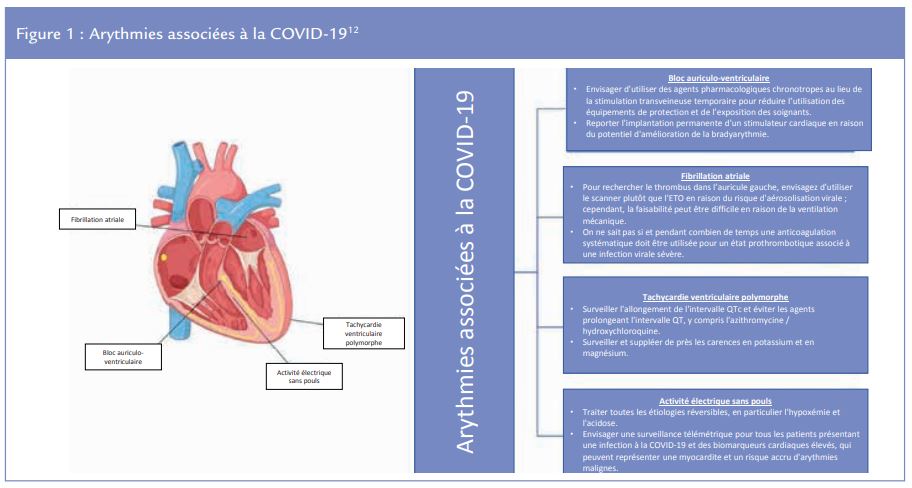
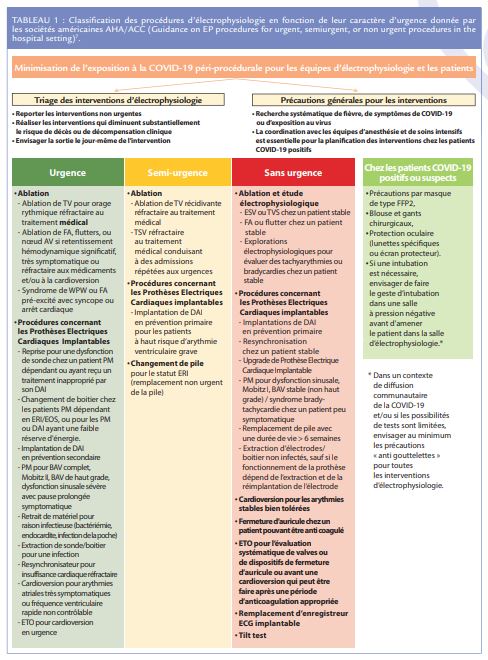
En cas de FA de survenue récente mal tolérée hémodynamiquement la cardioversion est conseillée et si le risque de récidive est très élevé en raison de la sévérité de l’état du patient, on pourra opter pour de l’amiodarone. Lorsque la FA est mieux tolérée, on peut être amené à privilégier le contrôle de la fréquence à celle du rythme pendant la période COVID-19, en évitant néanmoins un ralentissement trop marqué en cas de co-prescription des médicaments qui allongent le QT. En cas de flutter atrial, souvent plus difficile à ralentir que la FA, on privilégiera la cardioversion à l’ablation, qui devra se rediscuter ultérieurement (Tableau 2). Malgré une forte composante pro-thrombotique observée chez certains patients COVID-19 les indications de l’anticoagulation en cas de FA/flutter atrial restent celles défi nies dans les recommandations de l’ESC pour la population générale. Le choix de l’anticoagulant se fera en fonction de ses interactions avec les médicaments de la COVID-19 (notamment en ce qui concernent les AOD avec l’azithromycine (AZT), l’atazinovir, le lopinavir et le ritonavir), des autres indications au traitement anticoagulant (accidents thrombo-emboliques artériels ou veineux) et des défaillances rénales et hépatiques. Pour les arythmies ventriculaires soutenues de survenue récente la cardioversion s’impose en cas de mauvaise tolérance hémodynamique, sinon on privilégiera l’amiodarone.(Tableau 3)
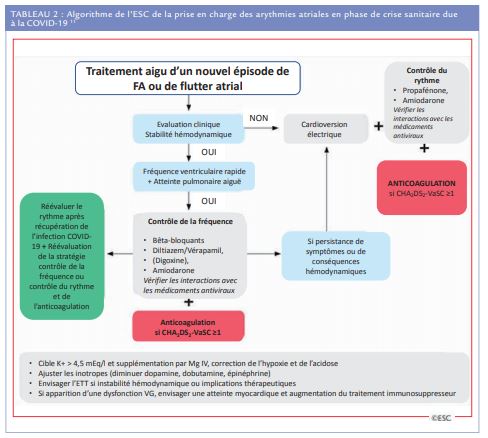
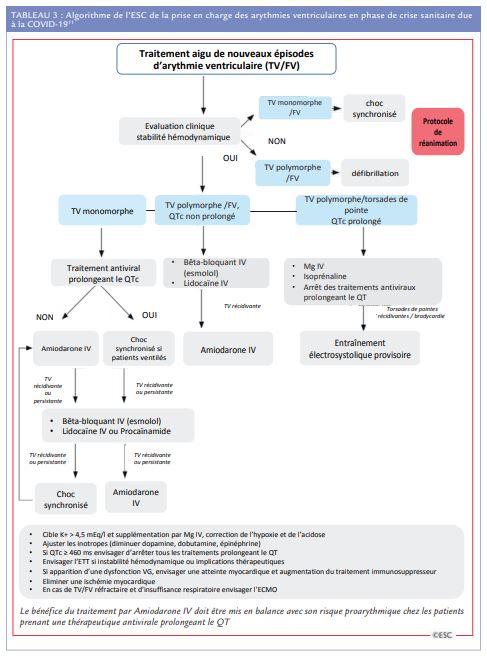
Dans tous les cas la co-prescription d’amiodarone et de médicaments de la COVID-19 qui allongent le QT devra se faire en prenant en compte le rapport bénéfice/risque de l’association. Enfin l’existence d’une canalopathie déjà connue, ou diagnostiquée à l’occasion de l’infection à SARS-CoV-2, doit faire adopter des mesures préventives pour réduire le risque d’arythmies ventriculaires graves (Tableau 4). Chez les patients ayant un syndrome de Brugada, ou des mutations portant sur les canaux sodiques, appareillés d’un défibrillateur il faut un contrôle rapide et complet de la fièvre par la prise précoce de paracétamol. Chez les patients connus comme à risque mais non-appareillés il convient de les hospitaliser avec une surveillance télémétrique continue jusqu’à la défervescence complète. La présence d’un syndrome du QT long congénital constitue quant à lui une contre-indication à l’administration des médicaments qui allongent le QT ou sinon et après discussion du rapport bénéfice/risque de les prescrire en unité avec une surveillance télémétrique continue. En cas de tachycardie ventriculaire catécholergique le traitement anti-arythmique notamment par bêta-bloquant doit être poursuivi en l’absence de défaillance hémodynamique sévère et l’adrénaline doit être évitée même en cas d’ACR.
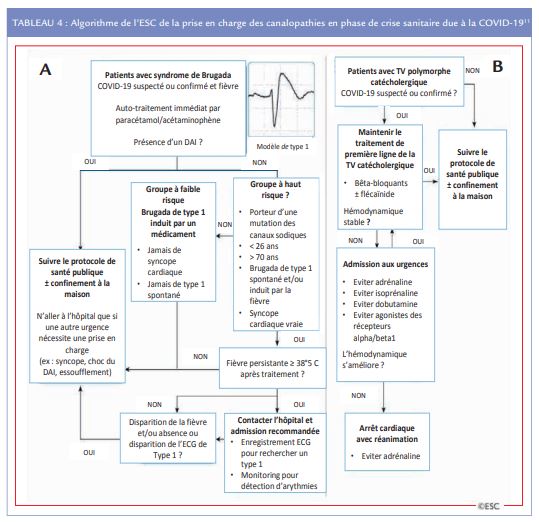
Interactions rythmologiques des médicaments proposés pour traiter la COVID-19
De nombreux médicaments ont été proposés pour le traitement de la COVID-19, dont le choix a été orienté par des hypothèses physiopathologiques, des données expérimentales ou des données cliniques observationnelles. Néanmoins à l’heure actuelle aucun de ces traitements n’a vu son efficacité sur la mortalité validée par des études prospectives randomisées, hormis la déxamethasone dans les formes respiratoires sévères. Ainsi en l’absence de preuve d’efficacité formelle il est fondamental de ne pas exposer les patients au risque potentiellement létal de leurs effets secondaires, qui peuvent résulter d’un effet électrophysiolgique direct ou d’une interaction pharmacodynamique avec les autres médicaments utilisés en cas d’arythmies (anti-arythmique et anticoagulant), par le biais des cytochromes P450 dont les CYP2D6 et les CYP3A4. Même si certains médicaments proposés dans la COVID-19 peuvent générer des troubles conductifs ou d’automatisme (Chloroquine Lopinavir/Ritonavir) la problématique s’est rapidement centrée sur l’allongement de l’intervalle QT et le risque d’arythmies ventriculaires polymorphes graves (notamment les Torsade de Pointes) qui lui est lié et peuvent être à l’origine d’ACR. Parmi les médicaments proposés dans la COVID-19 seuls la chloroquine (HQ), l’hydroxychloroquine (HCQ), l’azithromycine (AZ) (souvent en association avec l’HCQ) et certains antiviraux (Lopinavir/Ritonavir, Imatimib) sont connus pour allonger le QT. Cet effet résulte d’un blocage des canaux potassiques Kv11. (géne hERG-K+) pour l’HQ/HCQ ou d’une prolongation de la durée du courant sodique pour l’AZ. Par contre le Remdesivir et la Ribavirine ne paraissent pas modifier le QT, quant au Tocilizumab il pourrait même avoir un effet protecteur en s’opposant à l’allongement du QT induit par la cytokine IL-6 dont le taux plasmatique peut être largement augmenté dans l’infection à SARS-CoV-2.
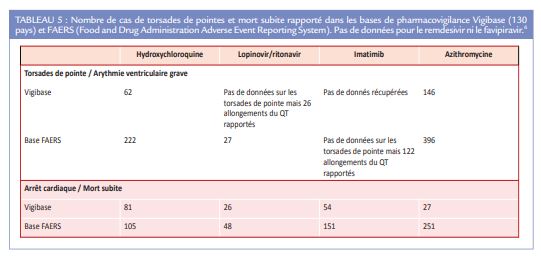
Deux grandes bases de pharmacovigilance, l’une américaine (FAERS) et l’autre de l’OMS (VIGIBASE), ont ainsi colligé les cas d’allongement du QT, de TdP et d’ACR rapportés lors de prescription d’HCQ, d’AZ, de l’association Lopinavir/Ritonavir et de l’Imatimib (Tableau 5), mais sans préciser leurs incidences qui paraissent néanmoins faibles en regard du volume estimé de prescription.
En réanalysant les données de la base de la FAERS Sarayani et al ont conclu qu’un signal d’alerte concernant les TdPs existait surtout pour l’AZ, mais il convient de prendre en compte que cette base ne comportait pas de patient COVID-19.
Plusieurs séries ont confirmé chez les patients COVID-19, suivis en ambulatoire ou hospitalisés, la réalité d’un allongement significatif du QTc avec l’HCQ, l’AZ et surtout avec l’association des deux. Ainsi l’allongement du QTc observé avec l’HCQ ou l’association HCQ+AZ, qui parait être maximal vers le 4ème jour, varie de 5 à 40 ms selon le statut clinique du patient, étant plus élevé chez les patients sévères que chez les patients moins graves. Le nombre de patients qui atteignent les valeurs seuils du QTc considérées comme étant à risque de TdP (QTc ≥ 500ms ou augmentation du QTC ≥ 60 ms par rapport au QTc pré-traitement) varie là encore de 4 à 8% selon leurs caractéristiques cliniques et le type de médicament (HQ, HCQ, AZ ou HCQ + AZ). Néanmoins cet allongement du QTc ne semble pas corrélé au risque de TdP.
Le risque rythmique lié à la prescription d’HCQ, d’AZ ou de leur association dans l’infection à SARS-CoV-2 a été évoqué dans une série rétrospective de 1 438 patients COVID-19 hospitalisés dans 25 hôpitaux de la métropole new-yorkaise et recevant soit de l’HCQ, soit l’association HCQ+AZ, soit de l’AZ seul, soit aucun de ces deux médicaments. Dans cette étude le taux d’ACR est plus élevé dans le groupe traité par l’association HCQ+AZ que dans le groupe ne recevant ni HCQ ni AZ. Néanmoins le mécanisme, rythmique ou non, de cet ACR, n’est pas précisé et par ailleurs il n’existe pas de différences entre les groupes en ce qui concerne les anomalies ECG (arythmies et allongement du QT).

Par contre dans d’autres séries et dans la revue de la littérature les cas documentés de TdP semblent peu fréquents (0 à 0,4%), alors que l’allongement du QT est présent chez des patients de 10 à 20 %. En fait la valeur du QTc est sensible mais peu spécifique pour prédire la survenue des TdP car la relation entre l’allongement du QTc et la survenue de l’arythmie n’est pas linéaire, et que la nature du médicament allongeant le QTc intervient également. Ainsi l’incidence des TdPs est plus élevée si le médicament qui allonge le QTc est un anti-arythmiques (1 à 5 %) que s’il ne l’est pas (0,001%).

Ainsi la survenue de TdP dans le cadre du QT long acquis résulte de l’association de deux ou plusieurs facteurs allongeant le QT dont les effets se potentialisent. Or cette condition se rencontre surtout chez les patients COVID-19 dont l’état clinique est sévère, surtout s’ils sont âgés, de sexe féminin avec la présence d’une cardiopathie préexistante, d’une hypokaliémie liée au SARS-CoV-2 ou aux diurétiques, d’une insuffisance rénale ou hépatique (entrainant une accumulation de l’HQ /HCQ), d’une atteinte myocardique directe, d’un taux élevé d’IL-6 dans le cadre de l’orage cytokinique qui allonge le QTc et de la co-prescription d’autres médicaments allongeant le QTc (https://www.covid19-druginteractions.org ; https://www.crediblemeds.org). Il pourrait s’y ajouter une prédisposition individuelle liée à un polymorphisme génétique portant sur les canaux potassiques, qui réduit la réserve de repolarisation sans anomalie évidente du QTc de base, mais qui entraîne une réponse excessive à un allongeur du QT.
L’incidence modérée des TdP chez les patients COVID-19 hospitalisés peut aussi s’expliquer en partie par le respect des préconisations émises par les différentes sociétés savantes cardiologiques fondées sur une bonne connaissance de la physiopathologie des TdP sur QT long acquis, et par la durée courte du traitement (5 à 10 jours).
La Société Française de Cardiologie propose une prise en charge différenciée en fonction d’éléments cliniques, dont la gravité des patients (ambulatoires ou hospitalisés), biologiques (au minimum kaliémie et créatinémie) et les co-prescriptions . (Tableaux 6A et 6B)
Pour les patients ambulatoires de moins de 65 ans ayant déjà eu un ECG, sans comorbidité cardiaque, hépatique, digestive ou rénale majeure et en l’absence d’autre médicament allongeant l’intervalle QT, un ECG peut n’être fait que s’il est facilement réalisable mais il devient obligatoire en cas de co-prescription de deux médicaments allongeant le QT. La fréquence et le mode de surveillance ECG après mise en route du traitement dépendra du contexte : patient ambulatoire ou hospitalisé en médecine ou en soins intensifs/
réanimation avec la surveillance télémétrique continue .
Cet ECG de contrôle permettra aussi de dépister d’éventuels troubles conductifs qui ont été décrit avec l’HQ et l’HCQ, mais qui surviennent habituellement lors de prise plus prolongée. Par ailleurs la correction des facteurs favorisants associés est fondamentale : hypokaliémie (<3,5 mmol/L), hypocalcémie (<2,2 mmol/L), hypomagnésémie, bradycardie inférieure à 50/mn, co-prescription de médicaments qui allongent le QT.
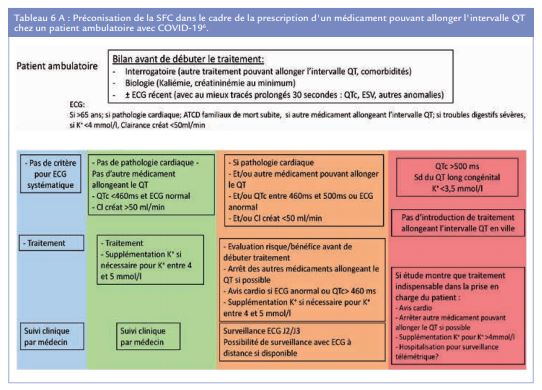

Les auteurs fixent le seuil du “QTc normal” comme étant inférieur à 460 ms, indépendamment de l’âge et du sexe. Ils préconisent d’éviter la prescription du médicament pouvant allonger l’intervalle QT pour un QTc supérieur ou égal à 500 ms. Au-delà de cette valeur la prescription ne pourra s’envisager qu’après avoir discuté du rapport bénéfice/risque entre les différents thérapeutes (cardiologue, infectiologue et réanimateur) et en s’entourant des précautions habituelles (maintien d’une kaliémie supérieure à 4 mmol/L, correction d’une hypocalcémie, éviction ou remplacement de tout autre médicament non indispensable allongeant l’intervalle QT (présents sur le site www.crediblemeds.org ou www.covid19-druginteractions.org) en favorisant une fréquence cardiaque supérieure à 50/mn et bien sûr en télémétrant le patient de façon continue.
Chez les patients qui ont un QTc de base supérieure à 460 ms mais inférieur à 500 ms, un contrôle ECG au 2ème/3ème jour avec un enregistreur ECG conventionnel ou avec un système ECG connecté validé doit être réalisé pour calculer le QTc. Sauf cas particulier un QTc supérieur à 500 ms, ou un allongement du QTc de plus de 60 ms par rapport au QTc pré-traitement, ou la survenue d’arythmie ventriculaire doit faire arrêter le traitement en ambulatoire, demander un avis cardiologique et entraîner une surveillance télémétrique urgente en milieu spécialisé si le traitement doit être continué car jugé vital.
La prise en charge d’une TdP passe quant à elle par l’administration intraveineuse (IV) de sels de magnésium en bolus, par la correction d’une hypokaliémie, et si besoin l’accélération de la fréquence cardiaque par l’isoprénaline ou la stimulation cardiaque transitoire. L’administration IV de lidocaïne a pu être proposée pour raccourcir le QT en aigu. Ces mesures doivent être associées à l’arrêt de tous les médicaments qui allongent le QT et à l’optimisation des paramètres hémodynamiques et ventilatoires, autant que faire se peut. Enfin les médicaments utilisés dans le traitement de la COVID-19 peuvent par le biais de leurs interactions avec les cytochromes P450 notamment le CYP3A4 et le CYP2D6, modifier les concentrations plasmatiques des anti-arythmiques et des anticoagulants, exposant ainsi à des « surdosages » ou au contraire à une diminution d’efficacité. On peut retrouver l’ensemble des interactions observées entre les différents médicaments qui sont utilisés chez les patients atteints de la COVID-19 sur le site de l’ANSM : https://www.ansm.sante.fr/Sinformer/Points-d-information-Points-d-information/ Medicaments-utilises-chez-les-patients-atteints-duCOVID-19-une-surveillance-renforcee-des-effetsindesirables-Point-d-information-actualise-le-14-05-2020
Influence de la pandémie sur la prise en charge des patients rythmologiques
Comme pour les autres spécialités cardiologiques la pandémie a eu de nombreux effets sur la prise en charge des patients de rythmologie. Du fait de la crise sanitaire qu’elle a créée, elle a impacté l’activité de rythmologie, d’une part en réduisant le nombre de procédures interventionnelles, essentiellement au détriment des ablations non liées à des orages rythmiques, mais aussi des implantations urgentes de prothèses électriques d’autre part en diminuant le nombre de consultations et d’hospitalisations conventionnelles. Cette réduction d’activité a résulté, non seulement des contraintes techniques (réorientation du matériel, des locaux et du personnel, protocoles de protection des soignants et des patients), mais aussi de la crainte des patients d’être hospitalisés dans une structure considérée “en surcharge” ou comme une source potentielle de contamination par le SARS-CoV-2. Elle a eu pour conséquence un retard de prise en charge de certaines arythmies, telle la FA et a pu participer à l’augmentation de la mortalité subite observée pendant la période de confinement.
L’un des rares effets positifs que l’on puisse attribuer à cette crise sanitaire a été le développement de la télémédecine qui a été largement valorisée. Si elle est parfaitement adaptée pour le suivi des prothèses électriques cardiaques implantables ou celles des patients ayant déjà eu un ECG, en s’aidant des enregistreurs ECG sans fi l connectés , elle reste moins adaptée pour une première consultation de rythmologie en raison de l’absence d’enregistreur ECG douze dérivations. La téléconsultation nécessite néanmoins une participation active du patient et la diffusion des systèmes de télétransmission chez le patient et dans la structure de soins. En cette période de circulation persistante du virus la téléconsultation constitue un atout major qui permet de réduire les déplacements et les contacts entre les patients et les soignants et donc le risque de contamination.
En conclusion
Les troubles du rythme, tant atriaux que ventriculaires, font partie du tableau clinique de la COVID-19, notamment chez les patients dont l’état clinique est sévère. Mais plus qu’à une pathogénicité rythmologique spécifique du SARS-Cov 2, ils semblent dépendre des différents mécanismes physiopathologiques (infectieux, métaboliques, inflammatoires, ischémiques, dysfonctions endothéliale et neuro-végétative…) impliqués dans cette infection, et de la préexistence d’une cardiopathie structurelle ou électrique souvent présente chez les patients âgés atteints de comorbidités. En fait ces arythmies ne semblent pas être la cause première des ACR observés chez ces patients. Leur traitement doit s’intégrer dans la correction globale des dysfonctions associées. Quant aux risques rythmiques liés aux médicaments allongeant le QT qui ont été proposés pour le traitement du COVID-19, même s’ils n’apparaissent pas majeurs moyennant le respect des recommandations, ils doivent être mis en balance avec leurs bénéfices thérapeutiques encore incertains
Cette pandémie, de par la crise sanitaire qu’elle a créée à son pic, a modifié les conditions de prise en charge des patients rythmologiques. Il est encore trop tôt pour en évaluer le retentissement sur la mortalité rythmique. En favorisant d’une part l’utilisation des systèmes connectés pour le diagnostic des troubles du rythme et la surveillance des prothèses électriques et d’autre part le raccourcissement des durées d’hospitalisation pour un certain nombre de procédures interventionnelles, elle va accélérer la transformation de cette discipline de façon pérenne.
N°35 – Sept 2020
Thomas Lavergne, Pierre Baudinaud, Victor Waldmann, Eloi Marijon, Nicolas Danchin
HEGP, Paris
L’auteur déclare ne pas avoir de liens d’intérêt.
Les références citées sont à retrouver sur le site e-Cordiam.
