
Nouvelles recommandations ESC 2021 sur l’Insuffisance Cardiaque aiguë et chronique : que retenir en pratique clinique ?
Cinq années se sont écoulées depuis les dernières recommandations de la Société Européenne de Cardiologie (ESC) sur l’insuffisance cardiaque (IC).1 Il était donc nécessaire de les actualiser à la suite des résultats positifs de plusieurs essais thérapeutiques.2–4 Nouvelles molécules, nouveaux concepts en IC, prise en charge personnalisée : cet article vous propose un résumé des recommandations ESC 2021 et tente d’en extraire les points essentiels pour la bonne pratique clinique.
Définition et diagnostic
La définition « historique » ne change pas. Parler d’IC nécessite la présence de symptômes et/ou des signes physiques d’IC avec la preuve d’une anomalie structurelle et/ou fonctionnelle cardiaque ayant pour conséquence une élévation des pressions intracardiaques et/ou une inadéquation du débit cardiaque au repos et/ou à l’effort.
Même si la FEVG reste la « pierre angulaire » pour classifier les patients, la terminologie a quelque peu changé. On parle désormais d’IC :
– à fraction d’éjection ventriculaire gauche (FEVG) réduite ≤ 40% (IC-FER),
– à FEVG préservée ≥ 50% (IC-FEP),
– et enfin d’IC à FEVG moyennement réduite (IC-FEmR) : « midly reduced » et non plus « mid range » quand la FEVG est entre 41 et 49%.
Ce changement a été proposé puisque certaines études suggèrent que les traitements de l’IC-FER pourraient être bénéfiques dans ce cas.5–8
La stratégie de confirmation diagnostique de l’IC recommandée par l’ESC est présentée Figure 1.
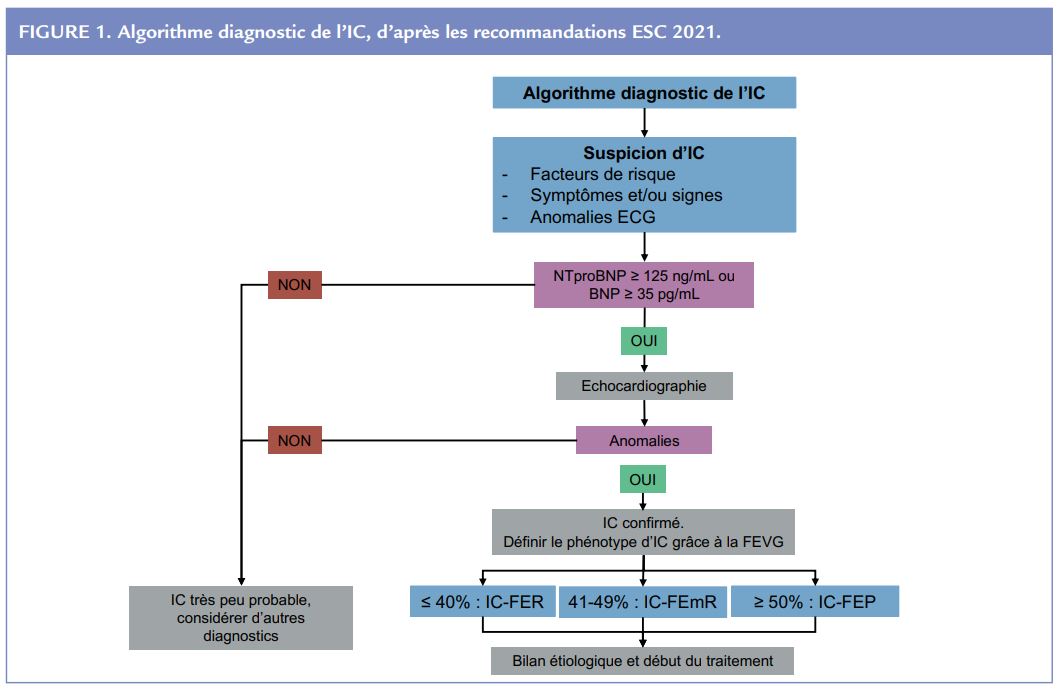
En continuité du diagnostic positif, la place des examens complémentaires pour le diagnostic étiologique est aussi précisée :
- La réalisation d’un cathétérisme cardiaque droit :
- doit être considérée en cas de suspicion de péricardite chronique constrictive, de cardiomyopathie restrictive, de cardiopathie congénitale ou de suspicion de cardiopathie d’hyper débit (classe IIa)
- et peut être considérée en cas de suspicion d’IC-FEP pour confirmer le diagnostic (classe IIb).
- En cas de suspicion forte d’hypertension pulmonaire liée à l’IC gauche (groupe II), le grade de recommandation passe d’un niveau IIa à IIb en l’absence de traitement spécifique à proposer.
- Le coroscanner passe d’un niveau de preuve IIb à IIa en cas de probabilité pré-test faible à intermédiaire de coronaropathie.
- Au contraire, la coronarographie passe d’un niveau IIa à IIb en cas de probabilité pré-test intermédiaire à élevée de coronaropathie et la preuve d’une ischémie documentée.
- L’IRM cardiovasculaire garde sa place pour la caractérisation tissulaire myocardique et peut être considérée pour distinguer cardiopathie ischémique de non ischémique (classe IIa) sans toutefois qu’aucun seuil de rehaussement tardif ne soit encore proposé.
Insuffisance cardiaque chronique à FEVG ≤ 40%
Les nouvelles recommandations distinguent deux aspects dans la prise en charge qu’il faudra bien garder à l’esprit (Figure 2).
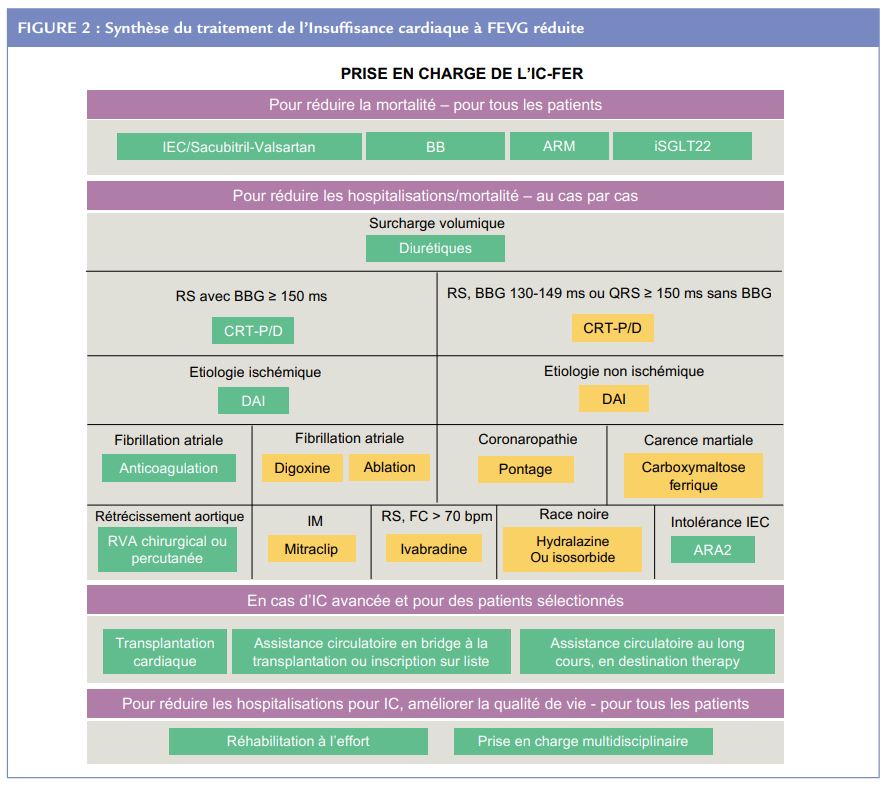
Prise en charge pour tous !
Tout d’abord, celle qui concerne l’ensemble des patients IC-FER et qui est associée à une réduction de la mortalité toute cause.
En 2016, c’était l’association Sacubitril/Valsartan qui faisait son entrée1 . En 2021, ce sont les glifl ozines (= inhibiteurs SGLT2) qui s’ajoutent à l’arsenal thérapeutique déjà existant, fort des résultats des études DAPA-HF et EMPEROR-REDUCED.2,4
Les inhibiteurs de l’enzyme de conversion (IEC) ou l’association Sacubitril/Valsartan, les béta-bloquants, les antagonistes des récepteurs aux minéralocorticoides (ARM) et les glifl ozines sont recommandés chez tous les patients, en première ligne, car associés à une réduction de la mortalité toutes causes et des hospitalisations pour IC (classe I).
Il est important de souligner que, contrairement à 2016, où il existait une escalade dans l’instauration des traitements (stratégie de traitement séquentiel : bithérapie par bétabloquants et IEC puis ajout d’un ARM 3 mois plus tard si la FEVG était toujours < 35%), ces nouvelles recommandations suggèrent de débuter l’ensemble des traitements, en même temps, à faible dose, puis de les titrer progressivement (stratégie de traitements combinés).
Prise en charge au cas par cas !
En parallèle des thérapeutiques décrites ci-dessus, certains traitements sont à envisager en fonction du phénotype des patients et permettent une réduction des hospitalisations pour IC et/ou de la mortalité cardiovasculaire.
Ainsi, le vericiguat, stimulateur de la guanylate cyclase, fait son entrée dans les recommandations suite aux résultats de l’étude VICTORIA.3 Celui-ci est indiqué chez les patients classe NYHA ≥ II, toujours symptomatiques malgré une trithérapie par IEC (ou sacubitril/valsartan), ARM, bétabloquants pour réduire la mortalité cardiovasculaire ou l’hospitalisation pour IC (classe IIb).
Les autres traitements tels que les diurétiques, les antagonistes du récepteur de type I à l’angiotensine II, les bloqueurs des canaux If et enfin la digoxine gardent les mêmes grades de recommandations.
Concernant la carence martiale, celle-ci doit être corrigée par carboxymaltose ferrique IV, chez des patients récemment hospitalisés pour IC avec une FEVG ≤ 50% et une férritinémie < 100 ng/mL ou comprise entre 100 et 299 ng/mL avec un coefficient de saturation de la transferrine < 20%, pour réduire le risque de réhospitalisation pour IC (classe IIa).
Concernant le traitement « électrique » de l’IC, on notera que :
- En prévention primaire, le défibrillateur automatique implantable est conforté en niveau de preuve I,A en cas de cardiopathie ischémique FEVG ≤ 35%, après 3 mois de traitement médical optimal, si le patient est toujours symptomatique classe II-III NYHA avec une espérance de vie > 1 an pour réduire le risque de décès toutes causes et de mort subite. Il est cependant rétrogradé en niveau de preuve IIa en cas de cardiopathie non ischémique.
- La resynchronisation elle aussi garde le même niveau de preuve (I,A) chez les patients avec une IC-FER ≤ 35%, en rythme sinusal, avec un bloc de branche gauche ≥ 150 ms malgré un traitement médical optimal d’au moins 3 mois pour réduire la morbi-mortalité alors qu’elle est dégradée à un niveau de preuve IIa en cas de bloc de branche gauche entre 130 et 149 ms contrairement à 2016.
- Le niveau de preuve de l’up-grading chez un patient déjà porteur d’un stimulateur cardiaque vers un CRT-P en cas d’IC-FEVG ≤ 35% sous traitement médical optimal passe d’un niveau II,b à II,a.
En cas de présence d’une valvulopathie, les recommandations réinsistent sur la nécessité de mise en place d’une « heart team ».
Concernant l’insuffisance mitrale (IM), la réparation percutanée bord à bord doit être considérée en cas d’IM secondaire, chez les patients non éligibles à une chirurgie, ne nécessitant pas de revascularisation coronaire, toujours symptomatiques malgré un traitement médical optimal et remplissant les critères suivants : FEVG 20-50%, DTSVG < 70 mm, PAPs < 70 mm Hg, absence de dysfonction modérée à sévère ventriculaire droite ou d’IT sévère, absence d’instabilité hémodynamique (grade IIa). En l’absence de ces critères, la recommandation est de grade IIb.
Enfin, la prise en charge de la fibrillation atriale occupe aussi une place importante de ces recommandations. La supériorité des AOD sur les AVK est confortée (classe I,A) pour ce qui est de l’anticoagulation. Concernant la prise en charge rythmique, en l’absence d’instabilité hémodynamique, les béta-bloquants sont recommandés en première intention (classe IIa) pour contrôle de la fréquence cardiaque, suivis des digitaliques et en cas d’association clairement établie entre FA paroxystique ou persistante et aggravation de l’IC persistante malgré traitement médical, l’ablation de FA doit être considérée (classe IIa) afi n de rétablir un rythme sinusal.
Insuffisance cardiaque chronique à FEVG > 40%
A FEVG moyennement réduite …
Il est important de bien comprendre que, même s’il existe un certain degré de chevauchement (overlap), parmi les patients IC en fonction de la FEVG, les patients IC-FEmR ressemblent davantage aux patients IC-FER sur le plan du terrain (ce sont majoritairement des hommes, jeunes avec une coronaropathie sous-jacente) mais ils s’en distinguent par une mortalité qui semble plus faible qu’en cas d’IC-FER.
Excepté une recommandation de classe I pour les diurétiques qui permettent de décongestionner, les IEC, ARA2, béta-bloquants, ARM et enfin l’association sacubitril/valsartan sont recommandés, comme dans l’IC-FER mais avec un grade de recommandation IIb.
A FEVG préservée…
Éternel challenge, à la fois diagnostique et thérapeutique pour les cardiologues du monde entier, l’IC-FER reste encore une fois le « parent pauvre » de ces recommandations. Alors que plusieurs scores ont été proposés pour une aide au diagnostic (H2FPEF et HFAPEFF),9,10 les recommandations soulignent la variabilité de leur performance. Contrairement à l’IC-FER ou l’IC-FEmR, où seule la FEVG réduite permet, en plus des symptômes et signes d’IC de faire le diagnostic, il faudra ici s’attarder sur d’autres paramètres échocardiographiques qui sont : une hypertrophie ventriculaire gauche (masse VG ≥ 95 g/ m2 chez la femme ou ≥ 115 g/m2 chez l’homme avec une épaisseur pariétale relative > 0,42), une dilatation atriale gauche (> 34 ml/m2), E/e’ 9, PAPs estimée supérieure à 35 mm Hg ou une VmaxIT > 2,8 m/s et enfi n l’élévation sanguine des peptides natriurétiques.
Excepté les diurétiques qui gardent un niveau de preuve I pour réduire les symptômes et signes d’IC, aucun traitement ayant fait la preuve de son efficacité sur la morbi-mortalité ne fait son entrée dans ces recommandations. Néanmoins, l’étude EMPEROR-PRESERVED, 11 positive en cas de FEVG > 40% a été présentée durant le congrès 2021. Devant l’apport de ce nouveau traitement, un addendum aux recommandations sera publié très prochainement pour ajouter l’empagliflozine à l’arsenal thérapeutique de l’ICFEP. Enfin, la prise en charge des comorbidités et facteurs de risques cardiovasculaires reste une priorité chez ces patients (classe I).
Insuffisance cardiaque aiguë
Bien qu’aucune nouvelle molécule n’ait fait son apparition, il faut quand même noter quelques changements dans les niveaux de preuves de traitements déjà connus. L’association diurétique de l’anse et diurétique thiazidique en cas de congestion résistante voit son niveau de preuve augmenter de IIb à IIa.
Au contraire, l’utilisation de vasodilatateurs en situation aiguë pour améliorer symptômes et signes congestifs voit sa recommandation passer de IIa à IIb. Enfin, l’utilisation en routine d’opiacés n’est plus recommandée (III versus IIb en 2016) sauf chez des patients sélectionnés.
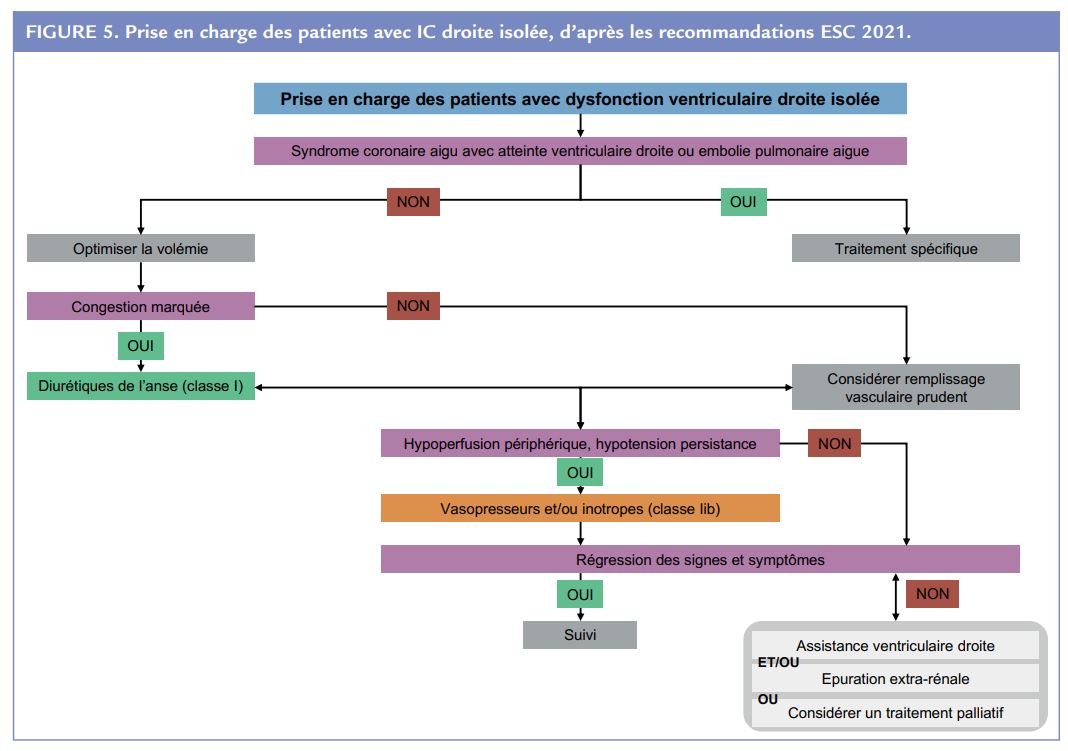
Très utile dans ces nouvelles recommandations, l’ESC propose plusieurs arbres décisionnels face à une insuffisance cardiaque aiguë (Figure 3), un choc cardiogénique (Figure 4) et une dysfonction ventriculaire droite isolée (Figure 5).
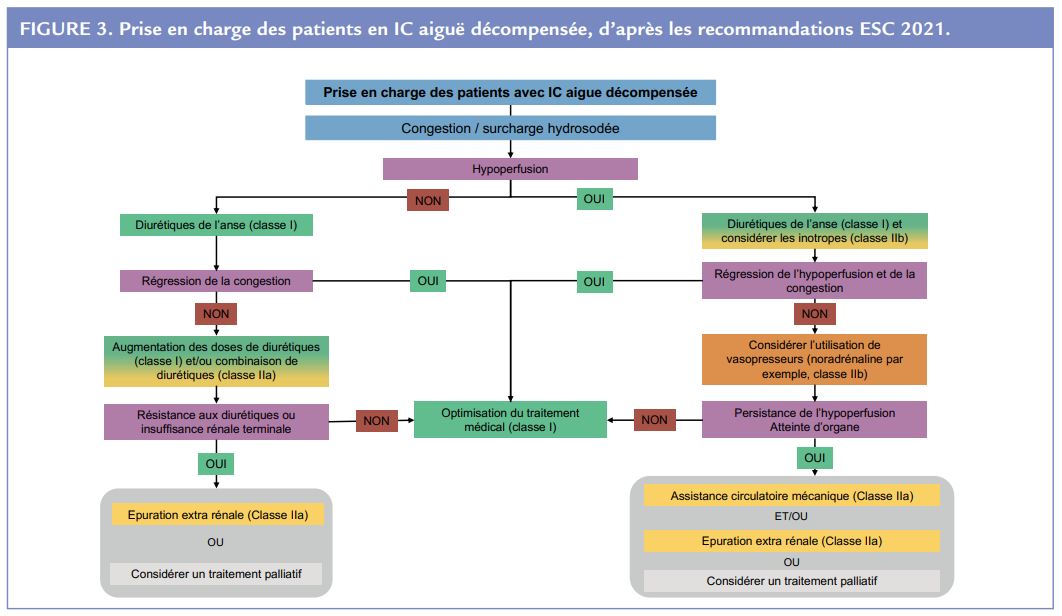
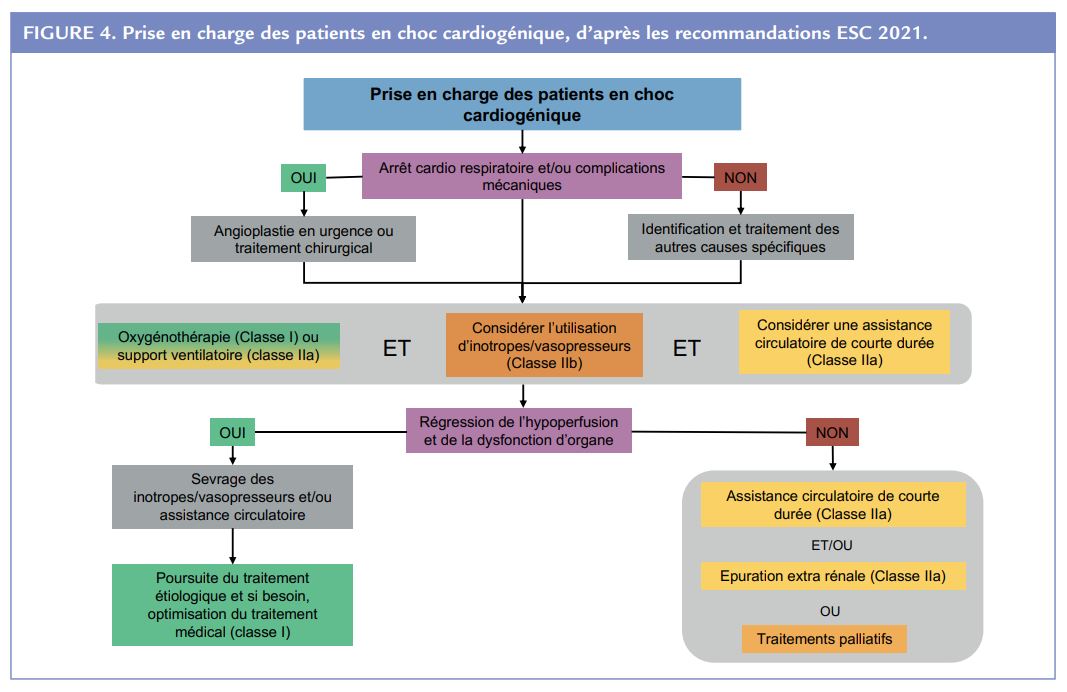
Insuffisance cardiaque avancée
Malgré le traitement médical décrit précédemment, certains patients restent symptomatiques et la maladie progresse vers l’IC avancée avec une mortalité à 1 an variant de 25% à 75%. 12 La définition de l’IC avancée reprise est celle proposée l’HFA (Heart Failure Association de l’ESC) en 2018 : 13 il faut la présence de tous les critères suivants malgré un traitement médical optimal.
- Classe III-IV NYHA
- Dysfonction cardiaque sévère définie par au moins 1 critère parmi :
- FEVG ≤ 30%
- Dysfonction VD isolée
- Valvulopathie sévère non opérable
- Cardiopathie congénitale sévère non opérable
- Taux élevés persistants ou augmentation du NTproBNP (ou BNP) et dysfonction diastolique sévère du VG ou anomalies structurelles VG (selon les définitions de l’IC-FEP)
- Épisode de congestion pulmonaire ou systémique nécessitant une forte dose de diurétiques IV ou des épisodes répétés de bas débit cardiaque nécessitant inotropes ou des amines vasoactives ou une arythmie maligne ayant entraîné> 1 hospitalisation dans les 12 derniers mois.
- Incapacité à l’effort sévère ou test de marche des 6 minutes < 300 m ou pic de VO2 < 12 ml/kg/min ou < 50% de la valeur prédite.
En plus de ces critères, des dysfonctions d’organes extracardiaques ainsi qu’une hypertension pulmonaire du groupe II peuvent être présentes mais non nécessaires pour poser le diagnostic.
Face à ces patients, la difficulté pour le clinicien est double : i) les identifier, ii) savoir les adresser vers un centre expert au bon moment et non trop « tardivement » comme c’est souvent le cas.
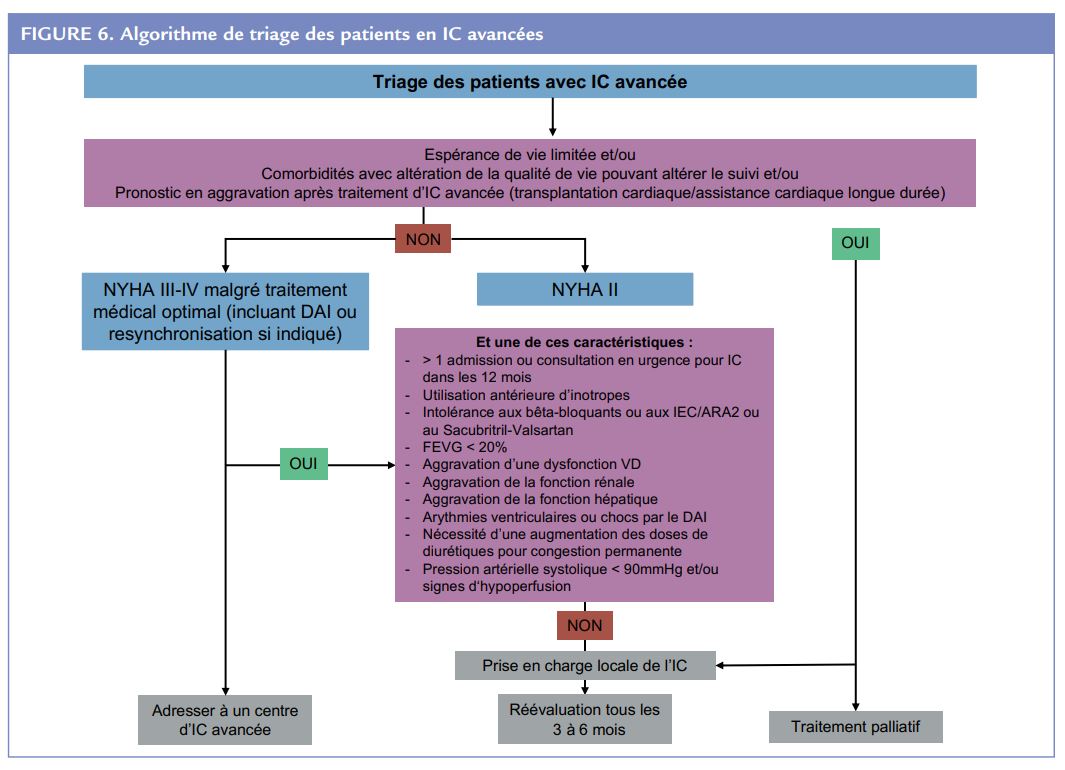
Ainsi, le triage est mis au centre de cette recommandations (Figure 6). En cas de classe fonctionnelle NYHA III-IV malgré un traitement médical optimal, la situation est aisée et l’adressage en centre expert doit être considérée. En cas de classe fonctionnelle NYHA II, identifier les « drapeaux rouges » est beaucoup plus complexe. Pour cela, les recommandations reprennent l’acronyme « I NEED HELP » proposé par Baunwol et al en 2017 :
I – Inotropes : utilisation d’inotrope par le passé
N – NYHA : classe III-IV NYHA et/ou élévation persistante des peptides natriurétiques
E – End-Organ Dysfunction : aggravation d’une insuffisance rénale ou hépatique
E – Ejection Fraction : FEVG < 20%
D – Defibrillator shocks : chocs récurrents appropriés du DAI
H – Hospitalizations : > 1 hospitalisation pour IC dans les 12 derniers mois
E – Edema/Escalating diuretics : congestion persistante et/ou nécessité d’augmenter les diurétiques
L – Low blood pressure : PAS < 90-100 mmHg
P – Prognostic medication : impossibilité de titrer ou nécessité de diminuer le traitement médicamenteux de l’IC
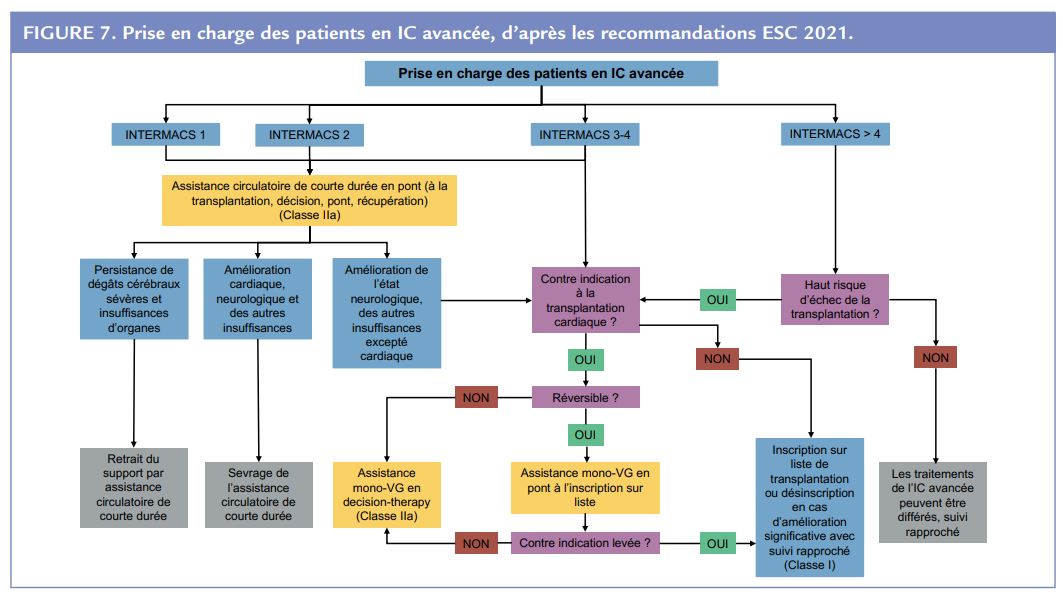
Enfin, la classification INTERMACS, initialement développée pour classer les patients ayant besoin d’une assistance circulatoire, doit être utilisée dans ce cas puisque c’est elle qui détermine la stratégie de prise en charge à suivre (Figure 7).
Conclusions et perspectives
L’arrivée successive de deux nouvelles classes thérapeutiques ayant un impact sur la mortalité toutes causes en cas d’IC-FER, au sein des deux dernières recommandations ESC sur l’IC prouve l’extraordinaire potentiel de la recherche cardiovasculaire.
Les recommandations 2021 sont riches en nouveautés et enseignements et cet article ne saurait les remplacer. La FEVG reste seule maître à bord pour classer les patients, probablement en décalage avec les outils non invasifs dont on dispose maintenant, qu’ils soient biologiques, échocardiographique, par IRM ou coroscanner.
Néanmoins, on notera que contrairement aux précédentes recommandations, les patients IC-FER doivent bénéficier d’une « quadrithérapie combinée » dont les doses doivent être augmentées progressivement et non plus d’un traitement « séquentiel » avec bi- puis trithérapie si besoin. Les modalités précises d’introduction (dans quel ordre plutôt qu’un autre ? tout le même jour ? etc…) et de titration ne sont néanmoins pas détaillées et d’autres études doivent s’y intéresser. La prise en charge « phénotypique » est aussi au cœur de ces nouvelles recommandations tout comme la nécessité de bénéficier d’une « Heart Team » pour prendre les bonnes décisions, au bon moment.
Charles Fauvel, CHU de Rouen
Théo Pezel, CHU Lariboisière – APHP, Paris
RÉFÉRENCES
1 Ponikowski P, Voors AA, Anker SD, et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Eur J Heart Fail. 2016;18(8):891-975.
- McMurray JJV, Solomon SD, Inzucchi SE, et al. Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction. N Engl J Med. 2019;381(21):1995-2008.
- Armstrong PW, Pieske B, Anstrom KJ, et al. Vericiguat in Patients with Heart Failure and Reduced Ejection Fraction. N Engl J Med. 2020;382(20):1883-93.
- Packer M, Anker SD, Butler J, et al. Cardiovascular and Renal Outcomes with Empagliflozin in Heart Failure. N Engl J Med. 2020;383(15):1413-24.
- Solomon SD, McMurray JJV, Anand IS, et al. Angiotensin-Neprilysin Inhibition in Heart Failure with Preserved Ejection Fraction. N Engl J Med. 24 2019;381(17):1609-20.
- Lund LH, Claggett B, Liu J, et al. Heart failure with mid-range ejection fraction in CHARM: characteristics, outcomes and effect of candesartan across the entire ejection fraction spectrum. Eur J Heart Fail. 2018;20(8):1230-9.
- Cleland JGF, Bunting KV, Flather MD, et al. Beta-blockers for heart failure with reduced, mid-range, and preserved ejection fraction: an individual patient-level analysis of double-blind randomized trials. Eur Heart J. 2018;39(1):26-35.
- Solomon SD, Claggett B, Lewis EF, et al. Influence of ejection fraction on outcomes and efficacy of spironolactone in patients with heart failure with preserved ejection fraction. Eur Heart J. 2016;37(5):455-62.
- Pieske B, Tschöpe C, de Boer RA, et al. How to diagnose heart failure with preserved ejection fraction: the HFA-PEFF diagnostic algorithm: a consensus recommendation from the Heart Failure Association (HFA) of the European Society of Cardiology (ESC). Eur Heart J. 2019;40(40):3297-317.
- Reddy YNV, Carter RE, Obokata M, et al. A Simple, Evidence-Based Approach to Help Guide Diagnosis of Heart Failure With Preserved Ejection Fraction. Circulation. 28 2018;138(9):861-70.
- Anker SD, Butler J, Filippatos G,et al. Empagliflozin in Heart Failure with a Preserved Ejection Fraction. N Engl J Med. 2021;
- McDonagh TA, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021;ehab368.
- Crespo-Leiro MG, Metra M, Lund LH, et al. Advanced heart failure: a position statement of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail. 2018;20(11):1505-35.
