
FRAME-AMI
Comparaison d’une stratégie guidée par FFR contre guidée par angiographie pour le traitement des patients avec infarctus du myocarde et maladie coronaire multi tronculaire. FFR Versus Angiography-Guided Strategy for Management of AMI With Multivessel Disease (FRAME-AMI)
Contexte et hypothèse
Un patient sur 2 admis pour un infarctus du myocarde est porteur d’une ou deux lésions coronaires, en plus de l’artère coupable de l’infarctus du myocarde. Les essais cliniques PRAMI, COMPLETE, CULPRIT, et DANAMI
PRIMULTI ont démontré qu’une revascularisation préventive de ces lésions complémentaires (sténose > 50 %) durant la même hospitalisation permettaient de réduire le risque de ré-infarctus du myocarde ou de décès cardiovasculaire1-4. En 2017, l’essai clinique COMPARE ACUTE a démontré qu’une stratégie de revascularisation guidée par FFR sur les lésions complémentaires était supérieure au traitement médical conservateur de ces lésions5. Ces résultats ont mené à une recommandation de rang I, niveau de preuve A, en faveur d’une revascularisation complète chez les patients admis pour STEMI6.
La question de comment guider les angioplasties préventives des lésions coronaires non-coupables s’est alors posée. La FFR est considérée comme la méthode invasive de référence pour dépister une lésion responsable d’ischémie chez les patients stables, permettant d’éviter les angioplasties inutiles et d’améliorer le pronostic des patients. Néanmoins, FLOWER-MI et FUTURE n’ont pas démontré la supériorité d’une revascularisation complète guidée par FFR chez les patients multi tronculaires admis pour infarctus du myocarde7,8.
Présenté par le Docteur Joo-Yong Hahn (Samsung Medical Center – Seoul, Corée), l’essai clinique FRAME AMI a pour objectif de comparer une stratégie guidée par FFR pour traiter les lésions non coupables chez les patients atteints d’ IDM en comparaison à une stratégie guidée par l’angiographie. L’hypothèse des investigateurs était qu’une stratégie guidée par FFR serait supérieure à une stratégie standard.
Critères d’inclusion
Les participants étaient des patients admis pour un SCA ST+ ou un SCA ST- avec succès de revascularisation de l’artère coupable, et une maladie multi-tronculaire défi nie par la présence d’une sténose complémentaire d’une artère coronaire de plus de 2 mm.
Les critères d’exclusions principaux étaient les suivants : patients en choc cardiogénique, présence d’une sténose complémentaire très serrée avec altération du flux, présence d’une occlusion chronique totale non accessible à l’angioplastie ou d’une lésion du tronc commun.
Plan d’étude et traitements étudiés
Il s’agit d’une étude randomisée, multicentrique, en ouvert, avec adjudication des évènements par un comité indépendant en aveugle.
La randomisation était stratifiée par centre, STEMI ou NSTEMI ou type de stents.
- Bras contrôle
- Angioplastie des lésions non-coupables guidée par l’angiographie (sténose > 50 %).
- Bras interventionnel
- Angioplastie coronaire guidée par FFR pour les sténoses non-coupables (> 50 % d’estimation visuelle) ; la FFR était effectuée par perfusion continue d’adénosine (140 ~ 180 ug/kg/min) ou par injection intracoronaire de nicorandil (bolus de 2 mg). En cad de FFR ≤ 0,80, une angioplastie était effectuée.
Critères de jugement
Le critère de jugement principal était le critère composite suivant : décès, infarctus du myocarde ou revascularisation répétée.
Les critères de jugements secondaires principaux étaient les évènements du critère composite pris séparément, ainsi que l’infarctus péri-procédural et la thrombose de stent.
Taille de l’échantillon et hypothèses statistiques
Le taux annuel attendu d’événements du critère de jugement était de 3,5 % avec la stratégie guidée par FFR et 6,0 % avec la stratégie guidée par angiographie, sur une durée de 3 ans.
En comptant 1 % de perdu de vue, il était prévu d’inclure 1 292 patients pour avoir une puissance de 90 % et un risque alpha de 5 %.
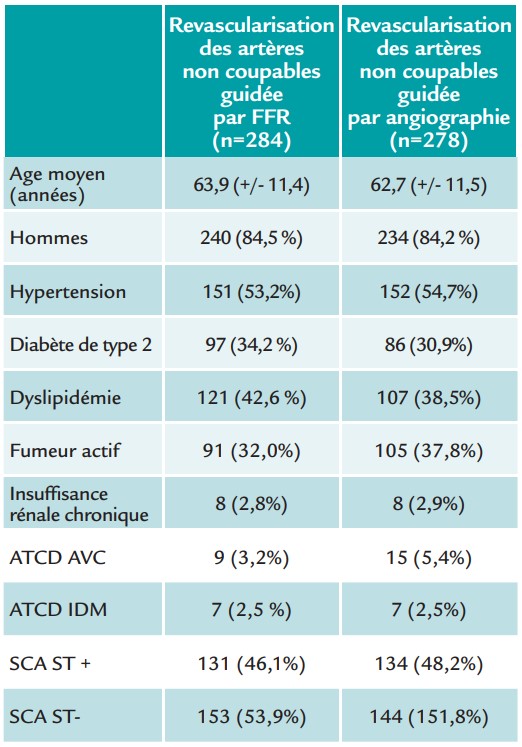
Population
Entre août 2016 et décembre 2020, un total de 562 patients ont été randomisés (contre 1 292 prévus initialement). L’essai a été interrompu prématurément pour faute de recrutement pendant la crise COVID 19.
L’âge moyen était de 63 ans et 16 % étaient des femmes. Environ 47 % des patients inclus étaient admis pour SCA ST+, et 53 % pour SCA ST-. Les lésions non coupables ont été traitées dans le même temps chez 60 % des patients et 40 % lors d’une deuxième procédure durant la même hospitalisation.
Dans le groupe standard, 97,1 % des lésions complémentaires ont été traitées, contre 64,1 % dans le groupe FFR. Le nombre de stent était également inférieur dans le groupe FFR.
Résultats
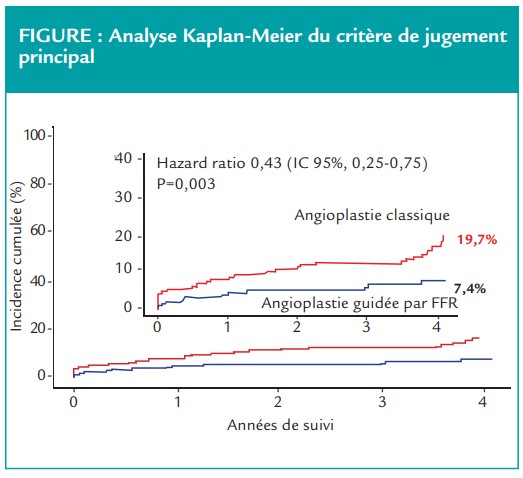
- Critère de jugement principal
Les résultats sont à interpréter avec prudence au vu de l’arrêt prématuré de l’essai clinique pour défaut de recrutement.
Avec un taux du critère de jugement composite de 7,4 % dans le groupe FFR contre 19,7 % dans le groupe ATL guidé par angiographie, la stratégie de revascularisation guidée par FFR semblait supérieure pour réduire les décès, infarctus ou revascularisation répétée [HR] 0,43 ; [IC] 95 % 0,25-0,75 ; p = 0,003)
- Critères secondaires
La stratégie de FFR contre angiographie donnait les résultats suivants
– Décès toute cause 2,1 % vs. 8,5 % p= 0,02
– Décès cardiovasculaire : 1,4 % vs. 8,2 %, p= 0,01 – Infarctus du myocarde : 2,5 % vs. 8,9 %, p=0,009
- Mortalité totale
Le décès toute cause est survenu avec un taux de 2,1 % dans le groupe FFR, contre 8,5 % dans le groupe ATL guidée par angiographie.
- Evénements indésirables et tolérance
Il n’y a pas eu de surrisque lié à la FFR.
Conclusion
Contrastant avec les résultats de FLOWER-MI et FUTURE, l’étude FFR-AMI a démontré une supériorité de l’usage de la FFR contre l’angiographie pour guider la revascularisation préventive des lésions non-coupables, chez des patients admis pour SCA ST+ et SCA ST-. Ces résultats étaient consistants pour les 2 présentations d’IDM, et montraient une diminution à la fois de la mortalité toute cause, de la mortalité cardiovasculaire et des infarctus du myocarde spontanés.
Il est difficile de tirer une conclusion de cet essai clinique, qui s’est arrêté prématurément à cause d’un défaut de recrutement lié au COVID 19 et il parait insuffisant pour changer les recommandations, comme l’a reconnu le Dr Hahn lors de la présentation en hotline. La mesure du flux coronaire en hyperhémie ne permet pas de prédire la rupture de plaque, il faut aussi considérer les caractéristiques anatomiques de ces plaques, leur localisation, et leurs caractéristiques
de vulnérabilité, chez des patients déjà sujets à l’athérothrombose. Néanmoins, il s’agit d’une première piste pour remettre la physiologie coronaire au cœur du traitement des patients complexes. « More research is needed… »
RÉFÉRENCES
1.K1. Engstrøm T, Kelbæk H, Helqvist S, et al. Complete revascularisation versus treatment of the culprit lesion only in patients with ST-segment elevation myocardial infarction and multivessel disease (DANAMI-3—
PRIMULTI): an open-label, randomised controlled trial. The Lancet 2015;386:665–71. doi:10.1016/S0140-6736(15)60648-1
2. Mehta SR, Wood DA, Storey RF, et al. Complete Revascularization with Multivessel PCI for Myocardial Infarction. New England Journal of Medicine 2019;381:1411–21. doi:10.1056/NEJMoa1907775
3. Wald DS, Morris JK, Wald NJ, et al. Randomized Trial of Preventive Angioplasty in Myocardial Infarction. New England Journal of Medicine 2013;369:1115–23. doi:10.1056/NEJMoa1305520
4. Gershlick AH, Khan JN, Kelly DJ, et al. Randomized Trial of Complete Versus Lesion-Only Revascularization in Patients Undergoing Primary Percutaneous Coronary Intervention for STEMI and Multivessel Disease.
J Am Coll Cardiol 2015;65:963–72. doi:10.1016/j.jacc.2014.12.038
5. Smits PC, Abdel-Wahab M, Neumann F-J, et al. Fractional Flow Reserve–Guided Multivessel Angioplasty in Myocardial Infarction. New England Journal of Medicine 2017;376:1234–44. doi:10.1056/
NEJMoa1701067
6. Ibanez B, James S, Agewall S, et al. 2017 ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation: The Task Force for the management of acute myocardial
infarction in patients presenting with ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J 2018;39:119–77. doi:10.1093/eurheartj/ehx393
7. Rioufol G, Dérimay F, Roubille F, et al. Fractional Flow Reserve to Guide Treatment of Patients With Multivessel Coronary Artery Disease. J Am Coll Cardiol 2021;78:1875–85. doi:10.1016/j.jacc.2021.08.061
8. Puymirat E, Simon T, de Bruyne B, et al. Rationale and design of the Flow Evaluation to Guide Revascularization in Multivessel ST-Elevation Myocardial Infarction (FLOWER-MI) trial. Am Heart J 2020;222:1–7.
doi:10.1016/j.ahj.2019.12.015
Michel Zeitouni, Sorbonne Université, Hôpital Pitié Salpetrière, Action Cœur
