
La fuite de la valve tricuspide : fonctionnelle (secondaire) certes mais tellement importante et avec tellement de nouvelles données !
La régurgitation tricuspide est une valvulopathie très fréquente1 et étroitement liée au pronostic des patients2 .
Introduction
L’insuffisance tricuspide primitive est rare. (≤10% des fuites tricuspides) Elle concerne les pathologies intrinsèques à l’appareil valvulaire ou sous valvulaire (syndrome carcinoïde, maladie d’Epstein, endocardite, …). Dans 90% des cas, elle est dite “fonctionnelle” ou “secondaire” à une autre cardiopathie. Enfin, La régurgitation tricuspide liée aux sondes endocavitaires est considérée comme une 3ème catégorie, distincte des deux autres par sa complexité3 .
Le traitement de l’insuffisance tricuspide secondaire repose en 1er lieu sur celui de la cause et sur l’optimisation de la volémie.
- Comme la fuite mitrale secondaire, il est essentiel de ne considérer la fuite tricuspide que lorsque le patient est médicalement stabilisé.
Dans les recommandations européennes de la Société de Cardiologie4 en cas de chirurgie valvulaire autre, si l’insuffisance tricuspide est moyenne à sévère ou associée à une dilatation annulaire > 41mm en ETT, il est nécessaire d’envisager un geste sur la valve tricuspide afin d’améliorer le pronostic des patients.
- Dans le cas de l’insuffisance tricuspide secondaire isolée, les résultats d’un geste chirurgical ne portant que sur la valve tricuspide sont décevants avec une morbi-mortalité atteignant 30% à 30 jours, chez des patients souvent fragiles, âgés, et ayant des comorbidités5 . De fait, le cardiologue a trop longtemps « négligé » cette valvulopathie ne sachant comment la prendre en charge. Et ce d’autant plus que longtemps, l’impact clinique est plutôt « contrôlé » par l’augmentation des diurétiques.
Depuis quelques années grâce aux travaux de la Mayo clinic6,7 en particulier mais aussi avec l’émergence de thérapies percutanées, il existe un regain d’intérêt pour la régurgitation tricuspide secondaire, dont les perspectives de correction semblent prometteuses en limitant les risques d’une chirurgie cardiaque8 . En raison d’études de plus en plus abondantes sur le sujet, de progrès techniques considérables dans l’imagerie multimodale, nous connaissons un renouveau dans la compréhension des mécanismes de l’insuffisance tricuspide secondaire qui apparaît alors plus complexe que prévu.
Anatomie fonctionnelle
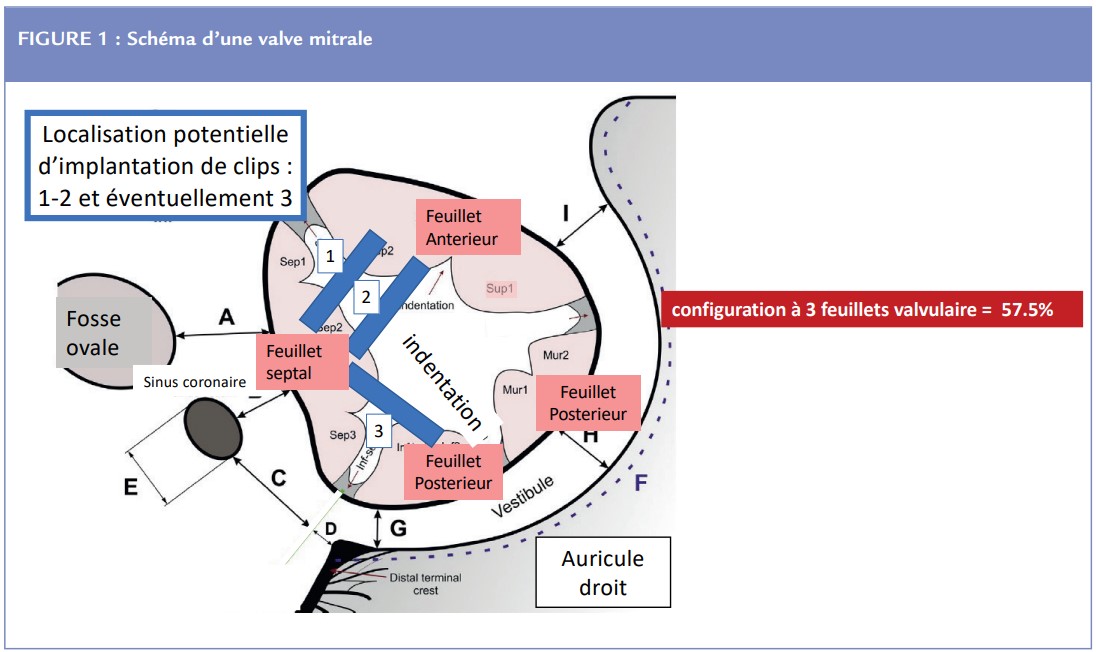
La valve tricuspide est une structure avasculaire membraneuse composée d’un anneau fibreux, feuillets, cordages et piliers. Son architecture en apparence superposable à celle de la valve mitrale présente plusieurs spécificités. Notamment il n’existe pas de continuité entre la valve tricuspide avec la valve ventriculo-artérielle correspondante (valve mitrale). Les cordages peuvent être directement ancrés dans la paroi ventriculaire (cordages septaux pour le feuillet septal en particulier). Classiquement décrit TRI-cuspide avec un feuillet antérieur, postérieur et septal, il a été démontré que cette anatomie n’est présente que dans 50% dans cas ; des conformations quadri voire pentacuspides sont décrites. Chacune des commissures ou indentations pouvant être le siège d’une fuite. La valve tricuspide possède en général 2 piliers (antérieur et postérieur) parfois un 3ème (septal) (Figure 1).
Les étiologies de la régurgitation tricuspide sont nombreuses et généralement liées à des modifications de l’environnement valvulaire : ventriculaire mais aussi souvent atrial (élargissement, aplatissement et sphérification de l’anneau tricuspide normalement en forme de selle de cheval). Elles peuvent être dues à une dilatation ventriculaire droite, dysfonction ventriculaire droite qu’elle soit globale ou segmentaire, une hypertension pulmonaire, une dilatation annulaire et parfois idiopathique (mais il faut comprendre pour pouvoir traiter !).
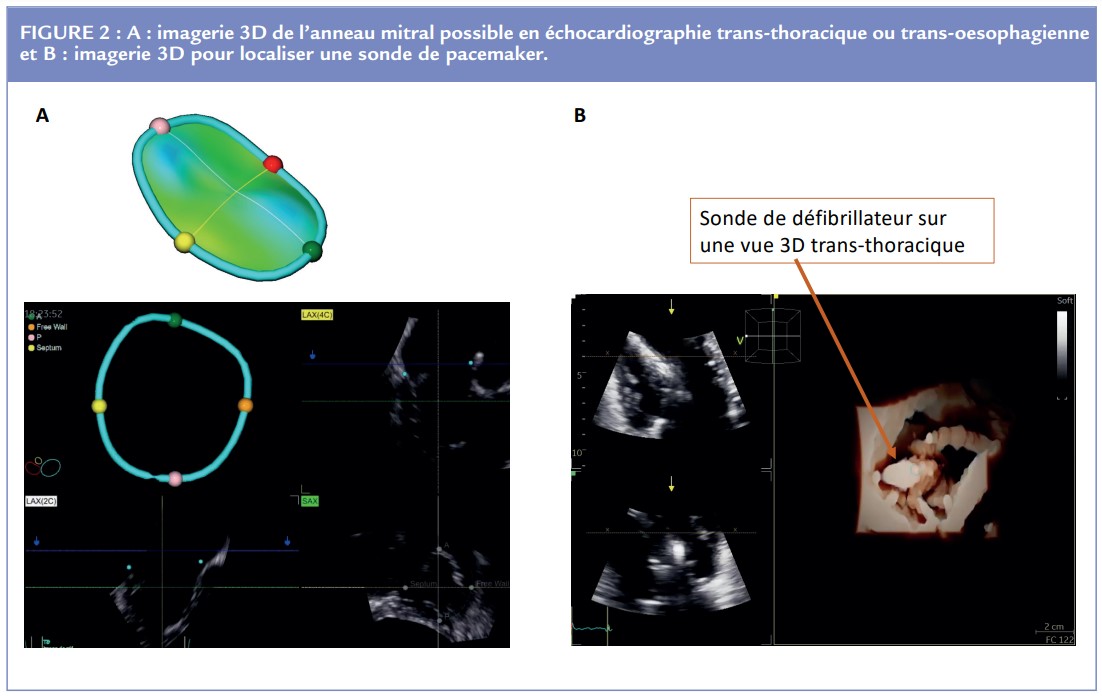
Bien qu’appelée “secondaire” la régurgitation tricuspide peut être isolée sans pour autant qu’il existe une atteinte structurelle valvulaire permettant de la classer en insuffisance « primitive ». Quelques études suggèrent un lien avec l’âge, la fibrillation atriale, le genre féminin : l’anatomie de l’anneau est dans ce cas, souvent la clé (Figure 2).
L’histoire naturelle de la régurgitation tricuspide est celle de l’auto-entretien et l’aggravation progressive.
- La valve tricuspide est très dépendante des conditions de charge.
En cas d’augmentation des pressions et volumes régnant dans les cavités droites, l’anneau tricuspide va se dilater au détriment de sa paroi latérale (la paroi septale étant plus rigide de par son contact avec les cavités gauches). L’anneau se déforme perdant sa conformation triangulaire en selle, pour une anatomie plus plane et circulaire. La dilatation ventriculaire entraine un « tenting » des feuillets valvulaires aggravant le défaut de coaptation et donc la fuite qui elle-même majore les conditions de charge des cavités droites1 .
- Il faut essayer de distinguer les régurgitations tricuspides plutôt d’origine atriale de celle dite ventriculaire (changement de géométrie, de taille et de fonction du ventricule droit. Rappelons que celui-ci est normalement triangulaire en vue apicale 4-cavités !).
- Ne pas se méprendre et analyser finement les fuites associées à des sondes de défibrillateur ou de stimulateur : elles sont fréquentes et potentiellement curables sans retirer la sonde (Figure 2).
Dans le cadre d’une insuffisance tricuspide atriale (idiopathie, fibrillation atriale), la géométrie standard triangulaire du ventricule droit est respectée outre une possible dilatation basale (Figure 3). Il n’existe alors pas ou peu de restriction valvulaire.
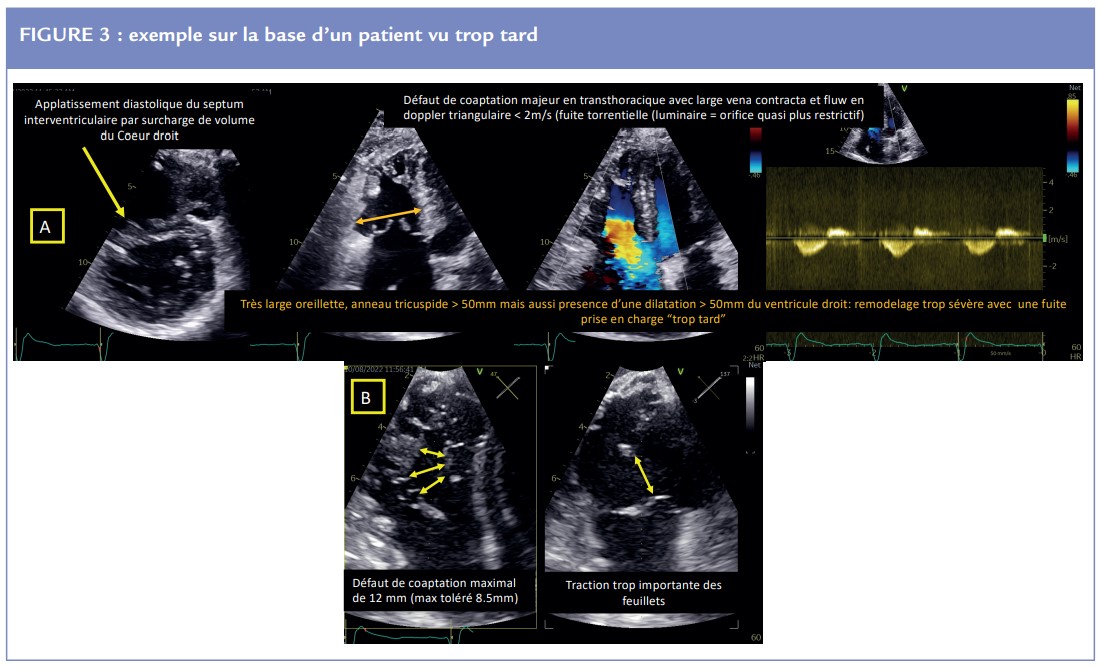
Dans le cadre d’une origine ventriculaire (hypertension pulmonaire, post infarctus), le ventricule droit apparaît dilaté et est à l’origine d’un « tenting valvulaire ».
L’évolution naturelle d’une fuite tricuspide tend vers une forme mixte : une dysfonction et dilatation ventriculaire droite liée à l’augmentation de la précharge ; une dilatation annulaire liée au reflux sanguin du ventricule droit vers l’oreillette.
- Agissons avant que le remodelage ventriculaire et atrial soit trop sévère ! (Figure 3).
L’analyse anatomique et fonctionnelle de la régurgitation tricuspide secondaire est complexe et devrait passer autant que faire se peut, par une évaluation multimodale. L’échocardiographie transthoracique est incontournable, elle pose le diagnostic, évalue la sévérité (5 stades), et permet une analyse du cœur gauche et des diamètres ventriculaires droits voire du tenting valvulaire sur une acquisition dédiée (apicale 4 cavités).
- L’analyse de l’insuffisance tricuspide secondaire ne doit pas être relayée au second plan.
Elle peut paraître difficile de prime abord mais certains indices peuvent alerter le praticien (défaut de coaptation,flux triangulaire, laminaire, reflux dans les veines sus hépatiques). Le calcul de la SOR et du volume régurgité par la PISA est en général plus aisé que dans les autres valvulopathies (Figure 3).
L’ETT présente plusieurs limites notamment sur le repérage spatial, de l’analyse fine valvulaire et sous valvulaire. L’échocardiographie transoesophagienne et l’échocardiographie 3D apportent de nombreuses réponses précises sur l’anatomie valvulaire et les possibilités de réparations.
L’IRM cardiaque a un intérêt dans les cas litigieux, elle permet d’évaluer la sévérité de la fuite par calcul de la fraction régurgitée mais surtout une analyse complémentaire de la fonction systolique ventriculaire droite. La présence de fibrose myocardique reste encore cliniquement difficile à affirmer. Le scanner cardiaque synchronisé quant à lui a surtout sa place dans le cadre des bilans préopératoires et de faisabilité d’implantation de dispositifs intracardiaques comme des valves percutanées (fusion scanner échocardiographie – Figure 4).
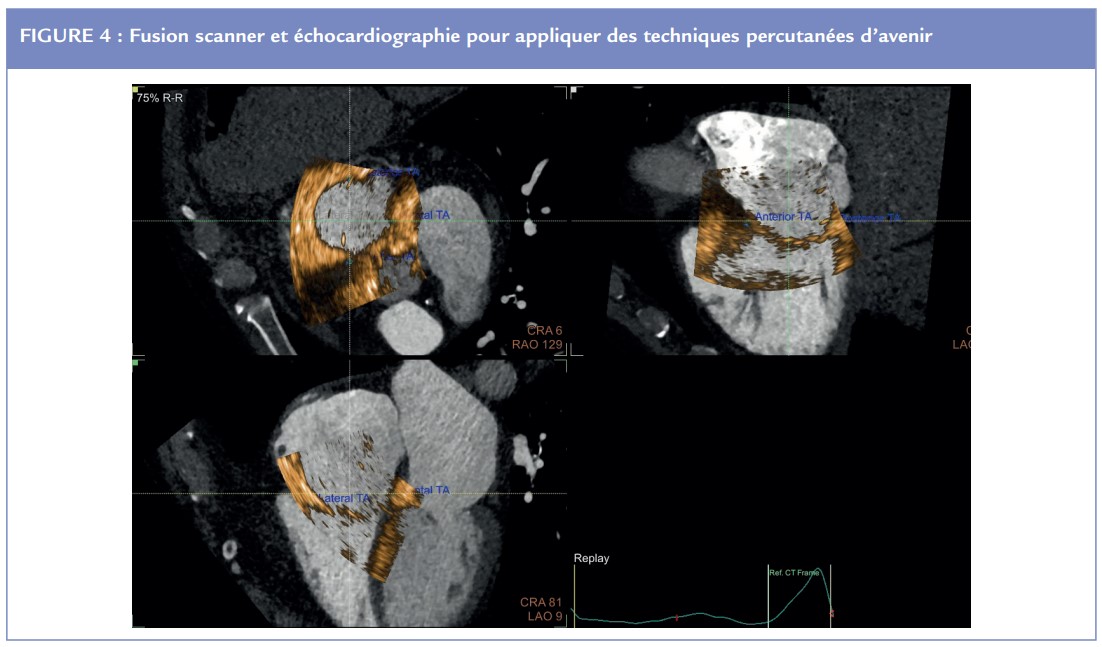
Perspectives de traitement
Longtemps le traitement interventionnel de référence reposait exclusivement sur la chirurgie conventionnelle par plastie ou remplacement valvulaire. Lorsqu’une chirurgie valvulaire autre est indiquée il est indispensable d’évaluer la valve tricuspide, en présence d’une fuite jugée moyenne à sévère ou d’une dilatation annulaire > 41mm il convient d’envisager un geste combiné pour améliorer le pronostic des patients. Les résultats étaient nettement plus mitigés dans le cadre de la fuite tricuspide secondaire isolée chez des patients fragiles et comorbides dont le bénéfice escompté d’une cure de la fuite tricuspide ne contrebalançait pas les risques d’une chirurgie cardiaque sous CEC. Le traitement reposait alors sur le contrôle de la volémie par les diurétiques avec un pronostic sombre.
- Apprécier le risque de la chirurgie : importance du TRI-score9
L’émergence récente de thérapies percutanées a finalement redistribué les cartes8 . Elles permettent d’envisager une correction de la régurgitation, toujours sous anesthésie générale (pour le moment), tout en permettant de surseoir aux complications de la sternotomie, de la circulation extracorporelle. La durée de l’intervention est plus courte avec une convalescence nettement plus rapide et des patients qui peuvent être levés dès le lendemain et rentrer à domicile en 48h. Actuellement plusieurs dispositifs sont à l’étude (clips, valves percutanées). Le plus utilisé à ce jour est le Triclip8 . La technique est proche de ce qui est fait avec le Mitraclip dans l’insuffisance mitrale. La procédure se fait par voie veineuse fémorale sous anesthésie générale et échoguidée par voie transoesophagienne. Le matériel utilisé a été développé spécifiquement pour la valve tricuspide. Les résultats semblent prometteurs et sont actuellement analysés dans le cadre de PHRC (triFR)8 . A ce jour, l’accessibilité à ces techniques dépend de protocole de recherche clinique.
- Il reste une difficulté pour la sélection des meilleurs candidats. Ne pas prendre en charge des patients trop sévères !
Les innovations thérapeutiques auront un intérêt pour des sujets n’ayant pas une pathologie valvulaire trop évoluée avec des conséquences irréversibles sur le myocarde. Quelques études abordent le sujet en essayant de stratifier la sévérité des conséquences de l’insuffisance tricuspide fonctionnelle avec certains paramètres semblant prometteurs (strain VD, strain OD, TAPSE/PAPs) et nettement plus altérés chez les patients aux plus mauvais pronostics. Il apparaît nécessaire que tout patient potentiellement éligible soit donc adressé tôt (et probablement avant que ces paramètres ne soient dégradés) en centre expert pour envisager une procédure10.
Conclusion
L’insuffisance tricuspide secondaire est une pathologie très fréquente et il faut retenir que son apparition constitue un tournant pronostique majeur.
Lorsqu’elle est associée à une autre valvulopathie, la chirurgie a toute sa place. Cependant, la chirurgie n’a pas fait totalement ses preuves dans le cadre de la fuite isolée. L’émergence des thérapies percutanées a permis un regain d’intérêt sur la compréhension de l’anatomie fonctionnelle aidée par l’évolution des techniques d’imagerie. Elles permettent d’envisager des traitements efficaces chez des patients à haut risque opératoire.
Nous ne pouvons plus nous permettre de négliger cette valvulopathie. L’analyse doit être fine, exhaustive, multimodale. L’une des difficultés sera la sélection des meilleurs candidats, comme dans toute valvulopathie, il faut suivre les patients, référés ceux-là pour un cathétérisme droit, une évaluation fonctionnelle et une imagerie d’expertise et sans doute, intervenir ni trop tôt ni trop tard.
Les auteurs déclarent ne pas avoir de liens d’intérêt vis-à-vis de cet article.
RÉFÉRENCES
- Guerin A, Dreyfus J, Le Tourneau T, et al. Secondary tricuspid regurgitation: Do we understand what we would like to treat? Arch Cardiovasc Dis 2019;112(10):642-651. DOI: 10.1016/j.acvd.2019.04.010.
- Topilsky Y, Inojosa JM, Benfari G, et al. Clinical presentation and outcome of tricuspid regurgitation in patients with systolic dysfunction. Eur Heart J 2018;39(39):3584-3592. DOI: 10.1093/eurheartj/ ehy434.
- Praz F, Muraru D, Kreidel F, et al. Transcatheter treatment for tricuspid valve disease. EuroIntervention 2021;17(10):791-808. DOI: 10.4244/EIJ-D-21-00695.
- Vahanian A, Beyersdorf F, Praz F, et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur J Cardiothorac Surg 2021;60(4):727-800. DOI: 10.1093/ejcts/ezab389.
- Dreyfus J, Flagiello M, Bazire B, et al. Isolated tricuspid valve surgery: impact of aetiology and clinical presentation on outcomes. Eur Heart J 2020;41(45):4304-4317. DOI: 10.1093/eurheartj/ehaa643.
- Benfari G, Antoine C, Miller WL, et al. Excess Mortality Associated With Functional Tricuspid Regurgitation Complicating Heart Failure With Reduced Ejection Fraction. Circulation 2019;140(3):196- 206. DOI: 10.1161/CIRCULATIONAHA.118.038946.
- Enriquez-Sarano M, Messika-Zeitoun D, Topilsky Y, Tribouilloy C, Benfari G, Michelena H. Tricuspid regurgitation is a public health crisis. Prog Cardiovasc Dis 2019;62(6):447-451. DOI: 10.1016/j. pcad.2019.10.009.
- Donal E, Leurent G, Ganivet A, et al. Multicentric randomized evaluation of a tricuspid valve percutaneous repair system (clip for the tricuspid valve) in the treatment of severe secondary tricuspid regurgitation Tri.Fr Design paper. Eur Heart J Cardiovasc Imaging 2021. DOI: 10.1093/ehjci/jeab255.
- Dreyfus J, Audureau E, Bohbot Y, et al. TRI-SCORE: a new risk score for in-hospital mortality prediction after isolated tricuspid valve surgery. Eur Heart J 2022;43(7):654-662. DOI: 10.1093/eurheartj/ ehab679.
- Vely M, L’Offi cial G, Galli E, et al. Functional tricuspid regurgitation: A clustering analysis and prognostic validation of three echocardiographic phenotypes in an external cohort. Int J Cardiol 2022. DOI: 10.1016/j.ijcard.2022.07.019.
Guillaume L’Official, Erwan Donal, CHU de Rennes
