
ECLS-Shock trial
Contexte et hypothèse
Le choc cardiogénique lié à l’infarctus du myocarde est la présentation la plus grave et péjorative des patients admis en cardiologie, avec une mortalité atteignant 50 % à 30 jours. Malgré des avancées majeures sur l’évaluation des meilleures stratégies de revascularisation, notamment l’étude SHOCK (1999) et l’étude CULPRIT-SHOCK (2017), la survie n’atteint qu’à peine 1 patient sur 2 admis en choc cardiogénique.
Chez les patients pour qui les mesures de réanimations standard ne permettent pas d’obtenir une stabilisation hémodynamique, l’assistance circulatoire mécanique par ECMO est disponible : elle permet de réduire la charge de travail ventriculaire et fournit un soutien hémodynamique assurant la perfusion des organes pendant la procédure d’angioplastie.
Le recours à l’ECMO dans le choc cardiogénique lié à l’infarctus du myocarde est en augmentation, en particulier aux USA, sans qu’aucun essai randomisé n’ait évalué son efficacité pour réduire la mortalité. De plus, l’ECMO est un dispositif invasif et à haut risque de complications des voies d’abord, de saignement ou d’accidents ischémiques, chez des patients souvent fragiles.
Ainsi, l’objectif de l’étude ELCS-SHOCK menée par la brillante équipe de l’institut cardiologique de Leipzig, avait pour objectif d’évaluer l’efficacité de la mise en place immédiate et systématique d’un ECMO pour les patients admis en choc cardiogénique lié à un infarctus du myocarde.
L’essai clinique a été soutenu par la Fondation Else Kröner Fresenius, la Fondation allemande pour la recherche sur le cœur et l’Helios Institut de santé (anciennement Institut de cardiologie de Leipzig).
Critères d’inclusion
Les patients inclus étaient âgés de 18 à 80 ans et présentaient un infarctus du myocarde compliqué d’un choc cardiogénique avec indication d’une revascularisation par angioplastie primaire ou pontage
aorto-coronarien.
Le choc cardiogénique était défini par les critères
suivants :
– Pression artérielle systolique inférieure à 90mm Hg pendant plus de 30minutes ou initiation de catécholamines pour maintenir une pression systolique supérieure à 90mmHg
– Un taux de lactate artériel supérieur à 3 mmol par litre
– Signes d’altération de la perfusion des organes avec au moins un des critères suivants : altération de l’état mental, peau et membres froids ou moites, ou débit urinaire inférieur à 30ml par heure.
Les critères d’exclusions étaient les suivants :
– Patients qui avaient subi une réanimation cardiopulmonaire pendant plus de 45 minutes avant la randomisation
– Cause mécanique de choc cardiogénique
– Maladie artérielle périphérique grave empêchant l’insertion de canules d’ECMO
Plan d’étude et traitements étudiés
ECLS-SHOCK est un essai clinique initié par l’investigateur, randomisé ouvert en 1:1, multicentrique effectué en Allemagne et Slovénie. La randomisation était stratifiée par centre.
Les évènements ont été adjudiqués par un comité indépendant d’adjudication des données.
Il y avait 2 bras de randomisation :
– Bras contrôle : traitement médical et réanimation standard.
– Bras interventionnel : implantation d’une ECMO pendant la coronarographie, de préférence avant l’angioplastie primaire, en plus des mesures médicales de réanimations standards. L’utilisation d’une gaine fémorale artérielle antérograde été recommandée pour réduire le risque d’ischémie des membres inférieurs.
Critères de jugement
Le critère de jugement principal d’efficacité était le décès toutes causes à 30 jours. Le critère de jugement principal de sécurité était les saignements modérés ou sévères (BARC 3 à 5), les AVC ou embolisation systémique, et les complications ischémiques vasculaires nécessitant une intervention ou une chirurgie.
Taille de l’échantillon et hypothèses statistiques
L’hypothèse était d’une mortalité de 35% dans le groupe ECMO et 49% dans le groupe contrôle. Sur la base d’un risqué alpha de 0,05, 394 patients étaient nécessaires pour avoir une puissance de 80% et exclure l’hypothèse nulle d’absence de différence entre les groupes. En comptant 6% de retrait de consentement, il était envisagé que 420 patients étaient nécessairespour évaluer le critère de jugement principal décès toutes causes.
Population
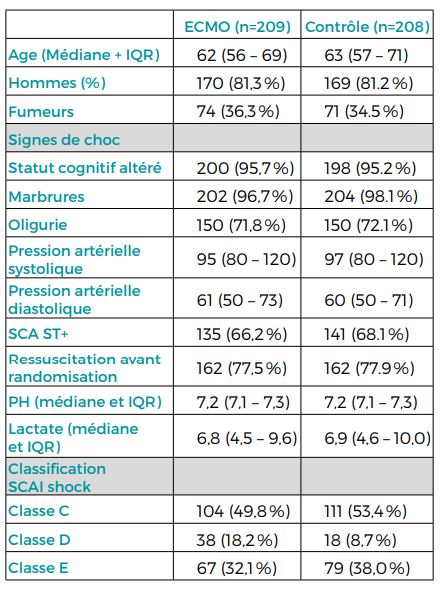
De juin 2019 à novembre 2022, un total de 420 patients (sur 844 évalués) ont été inclus dans 44 centres en Allemagne et Slovénie. Après exclusion de 3 patients pour retrait de consentement, il y avait 209 patients dans le groupe ECLS et 208 dans le groupe témoin.
Résultats
Critère de jugement principal :
À 30 jours, le décès toute cause est survenu chez 100 des 209 patients (47,8 %) dans le groupe ECMO et chez 102 patients sur 208 (49,0 %) dans le groupe témoin (tableau). RR = 0,98 ; 95 % IC 0,80 à 1,19 ; P=0,81
Critère de jugement de sécurité
Des hémorragies BARC 3 à 5 sont survenues chez 23,4% des patients du groupe ECMO et chez 9,6% de ceux du groupe témoin (risque relatif, 2,44 ; IC à 95%, 1,50 à 3,95 ). De même, les complications vasculaires périphériques justifiant une intervention sont survenues 11,0% et 3,8%, respectivement (risque relatif, 2,86 ; IC à 95%, 1,31 à 6,25).
La fréquence des accidents vasculaires cérébraux ou l’embolisation systémique était de 3,8% dans le groupe ECMO et 2,9% dans le groupe témoin (relatif risque, 1,33 ; IC à 95%, 0,47 à 3,76)
Analyses de sous-groupes
Les résultats étaient consistants dans tous les sous-groupes démographiques, quelles que soient la présentation initiale et la sévérité.
Conclusion
L’essai ECLS-SHOCK a démontré que l’ECMO mise enplace précocement et en routine chez les patients admis pour choc cardiogénique lié à un infarctus du myocarde n’améliorait pas le pronostic en comparaison à une réanimation standard : aucun effet n’a été observé sur la mortalité à 30 jours. De plus, l’ECMO était associée à une augmentation des complications de voie d’accès vasculaire et saignements. Ces résultats sont appuyés par une métanalyse impliquant ECLS-SHOCK et 3 autres essais cliniques parus dans le Lancet au même moment.
Il s’agit d’un essai clinique bien mené, avec des patients en choc cardiogénique graves (critères d’inclusions plus sévères que CULPRIT-SHOCK), avec 77% de ressuscitation avant admission, représentatifs de la population pour laquelle la problématique de l’assistance cardiaque par ECMO se pose dans les centres d’insuffisance cardiaque avancée.
L’essai ECLS-SHOCK fournit une réponse claire et solide concernant l’absence de bénéfices de l’ECMO en routine dans le choc cardiogénique lié à l’infarctus du myocarde. Il convient maintenant de développer les pistes de recherche et les stratégies pour diminuer la mortalité de cette pathologie qui continue à atteindre 50%.
